Abstract
Objectif: Réviser et développer l'édition 1996 des lignes directrices de pratique clinique de la Société de l'ostéoporose du Canada pour la prise en charge de l'ostéoporose en y intégrant les progrès récents du diagnostic, de la prévention et de la prise en charge de l'ostéoporose, et trouver et évaluer les données probantes à l'appui des recommandations.
Options: On a passé en revue tous les aspects des soins de l'ostéoporose et des complications qui en découlent en cas de fracture — y compris la classification, le diagnostic, la prise en charge et les méthodes de dépistage, ainsi que la prévention et la réduction du risque de fracture — pour les réviser au besoin et les exprimer sous forme d'une série de recommandations.
Résultats: Stratégies de repérage et d'évaluation des sujets à risque, utilisation de la densité minérale osseuse et des marqueurs biochimiques pour le diagnostic et l'évaluation de la réponse à la prise en charge, recommandations sur la nutrition et l'activité physique, et sélection d'une pharmacothérapie pour la prévention et la prise en charge de l'ostéoporose chez les hommes et les femmes, ainsi que de l'ostéoporose découlant d'un traitement aux glucocorticoïdes.
Données probantes: On a fondé toutes les recommandations sur un processus justifiable et reproductible mettant en cause une méthode explicite d'évaluation et de citation des données probantes à l'appui.
Valeurs: Les membres du Conseil consultatif scientifique de la Société de l'ostéoporose du Canada, un comité directeur d'experts et d'autres intervenants, y compris des médecins de famille, des diététistes, des thérapeutes et des représentants de diverses spécialités médicales qui s'occupent de traiter l'ostéoporose (médecine gériatrique, rhumatologie, endocrinologie, obstétrique et gynécologie, néphrologie, radiologie), ainsi que des spécialistes de la méthodologie de toutes les régions du Canada, ont passé en revue toutes les recommandations.
Avantages,réjudicest coûts: Le diagnostic plus rapide et la prévention des fractures devraient réduire les fardeaux médical, social et économique imposés par cette maladie.
Recommandations: Ce document présente un aperçu des recommandations détaillées portant sur tous les aspects de l'ostéoporose. On recommande des stratégies de repérage des sujets à risque accru (c.-à-d. ceux qui présentent au moins un facteur de risque majeur ou deux facteurs mineurs) et de dépistage par absorptiométrie centrale biénergétique à rayons X (DXA centrale) à 65 ans. Les bisphosphonates et le raloxifène constituent les thérapies de première intention dans la prévention et le traitement de l'ostéoporose postménopausique. Les œstrogènes et la progestine-progestérone constituent une thérapie de première intention dans la prévention et une thérapie de seconde intention dans le traitement de l'ostéoporose postménopausique. La calcitonine administrée par voie nasale est une thérapie de seconde intention dans le traitement de l'ostéoporose postménopausique. Même si l'on n'en a pas encore approuvé l'utilisation au Canada, on s'attend à ce que la hPTH(1-34) constitue un traitement de première intention de l'ostéoporose grave chez les femmes ménopausées. On ne recommande pas l'ipriflavone, la vitamine K, ni le fluorure. Les bisphosphonates constituent la thérapie de première intention pour la prévention et le traitement de l'ostéoporose chez les patients qui ont besoin d'une thérapie prolongée aux glucocorticoïdes et chez les hommes atteints d'ostéoporose. La calcitonine par voie nasale ou parentérale constitue un traitement de première intention contre la douleur associée aux fractures vertébrales aiguës. On recommande l'exercice avec impact et une prise de calcium et de vitamine D appropriée à l'âge pour prévenir l'ostéoporose.
Validation: Nous avons noté toutes les recommandations selon la valeur des données probantes. Si les preuves étaient insuffisantes et que les recommandations ne reposaient que sur un consensus, nous l'avons indiqué. Il faut considérer ces lignes directrices comme ayant un caractère évolutif et devant être actualisées à intervalles réguliers selon l'évolution du domaine.
L'ostéoporose est un des grands problèmes de santé publique qui se posent au Canada (et dans le monde) et sa prévalence s'accroÎt. Dans notre pays, environ une femme sur quatre et un homme sur huit en souffrent1. Puisqu'approximativement le quart de la population aura plus de 65 ans en 2041, on peut s'attendre à ce que l'incidence de cette maladie monte en flèche au cours des prochaines décennies2. Son importance sur le plan de la santé publique et son intérêt clinique résident dans les fractures qu'elle cause. Selon des estimations qui demeurent prudentes, une Caucasienne de 50 ans a un risque résiduel de 40 % de subir des fractures de la hanche, des vertèbres ou des poignets pendant le reste de sa vie3.
Cette lourde morbidité a des conséquences médicales, sociales et financières considérables. Nombre de fractures vertébrales sont occultes et asymptomatiques; elles sont toutefois associées à un taux de mortalité plus élevé, tout comme dans le cas des fractures de la hanche4,5,6. Ce taux s'élève en moyenne de 20 % dans l'année qui suit une fracture de la hanche7. En d'autres termes, le risque à vie de fracture de la hanche chez une femme est de un sur six et donc supérieur au risque à vie (un sur neuf) de cancer du sein; le taux de mortalité lié à la fracture de la hanche est aussi plus élevé8,9. Ajoutons que la moitié des femmes qui se fracturent la hanche ne peuvent recouvrer leur état fonctionnel antérieur et en viennent à dépendre d'autrui dans leurs activités quotidiennes. Environ 20 % d'entre elles auront besoin de soins de longue durée7.
Les dépenses directes les plus lourdes qu'entraÎne l'ostéoporose vont au traitement des fractures et de leurs séquelles. Bien qu'ils puissent difficilement être évalués avec précision, ces frais sont appréciables. Selon certaines estimations10, le coût total en soins aigus de l'ostéoporose (hospitalisation, clinique externe, pharmacothérapie) a excédé 1,3 milliard de dollars canadiens en 1993. Depuis dix ans, ces coûts n'ont cessé d'augmenter et, aux États-Unis, ils varient de 17 à 20 milliards de dollars canadiens par an. Cette flambée des coûts pourrait dépasser les moyens consacrés au traitement des fractures ostéoporotiques (chirurgie orthopédique, temps et espace à réserver en salle de chirurgie, programmes de rééducation, budgets de médicaments).
Bien que les fractures ostéoporotiques soient une grande cause de morbidité, d'invalidité et de mortalité, elles peuvent être prévenues. C'est dans cette optique que le Comité consultatif scientifique (CCS) de la Société de l'ostéoporose du Canada (SOC) a entrepris d'actualiser et d'élargir les déclarations de consensus1,11 de 1996 et d'ainsi les transformer en lignes directrices fondées sur des données probantes.
Méthodes
Démarche
En 1999, la SOC a créé, en consultation avec le Comité consultatif scientifique, un Comité directeur du projet de lignes directrices. Elle a relevé les domaines d'examen suivants pour l'étude de l'ostéoporose : facteurs de risque, diagnostic, nutrition, activité physique, pharmacothérapie et thérapies parallèles ou complémentaires. Ce comité formé de membres du CCS était chargé de diriger les travaux d'élaboration de lignes directrices. Soixante-cinq intervenants ont été associés à cette démarche : autres membres du CCS, omnipraticiens, diététistes, thérapeutes et représentants des diverses spécialités médicales traitant l'ostéoporose (gériatrie, rhumatologie, endocrinologie, obstétrique et gynécologie, néphrologie et radiologie) avec des experts en méthodologie de tout le pays. On les a répartis entre un certain nombre de comités sectoriels comprenant chacun de quatre à neuf membres et un président. Chacun de ces organes devait recenser les études existantes et élaborer des recommandations dans son domaine d'examen.
Les comités sectoriels ont d'abord dégagé les questions essentielles dont devaient traiter les lignes directrices relatives à leurs domaines d'examen respectifs. On a décidé de s'attacher à la prise en charge de l'ostéoporose primaire. Bien que n'ayant pas dressé un bilan en bonne et due forme des études portant sur les facteurs de risque ou la prise en charge de l'ostéoporose secondaire, les comités ont choisi de regarder certaines études jugées de premier plan dans ce domaine, et notamment les essais où l'on a évalué l'ostéoporose induite par les glucocorticoïdes. L'analyse des facteurs de risque a surtout porté sur les facteurs de risque de la fracture de fragilisation, laquelle est l'issue clinique la plus importante dans l'ostéoporose. Il n'y a donc pas eu de revue de littérature sur les facteurs de risque de la densité minérale osseuse (DMO) basse.
Suivant les orientations du Comité directeur, les comités sectoriels ont procédé à une vaste recension des articles traitant de chacune des questions. La recherche d'articles originaux et de comptes rendus s'est faite dans les bases de données suivantes : Medline, Embase, HealthStar, Cancerlit, Cinahl, Grateful Med, Toxline, Psychinfo et Cochrane Collaboration. Dans tous les comptes rendus, on a relevé les articles originaux cités. Dans chaque base de données, on a remonté le plus loin possible dans le passé et aussi poussé vers le présent jusqu'en mai 2000. De plus, on a choisi et pris en compte dans les lignes directrices un certain nombre d'études de grand intérêt et d'études charnières publiées après la date limite fixée. Le président d'un comité sectoriel et un autre membre ont examiné tous les résumés extraits pour juger de leur applicabilité à chaque question. Si un résumé ou un titre était considéré comme applicable, on obtenait l'article entier, on le numérotait et on le remettait à deux ou trois membres du comité aux fins d'examen.
On a ainsi extrait 89 804 résumés, pour lesquels on a obtenu 6941 articles complets à examiner. Deux ou trois examinateurs ont parcouru indépendamment chaque article en se reportant à cette fin à un formulaire type. Aux divers articles, ils ont attribué une valeur probante pour ce qui est de la question traitée et du modèle de l'étude (Tableau 1)12. En l'absence de consensus, les articles étaient soumis à un nouvel examen et, s'il n'y avait toujours pas de consensus, on demandait aux membres du Comité directeur de les étudier et de prendre une décision.
Table 1.
Les principes ayant présidé à l'élaboration des lignes directrices, à la notation de la valeur probante des articles d'intérêt et à l'établissement et au classement des recommandations sont tirés des études spécialisées sur l'application de lignes directrices13,14.
Une fois tous les articles de premier plan examinés et notés pour leur valeur probante, chaque comité sectoriel a passé les données en revue et énoncé des recommandations. On a évalué ces dernières en appliquant un système de notation de recommandations utilisé pour le diabète12, lequel tient compte tant de la valeur probante que du consensus dégagé par les spécialistes (Tableau 2). On donnait la note D aux recommandations qui ne reposaient que sur un consensus des membres du comité et pour lesquelles soit les données n'étaient pas clairement étayées par les faits, soit les données probantes étaient faibles. Avant d'y aller d'une note définitive, le Comité directeur a examiné toutes les recommandations en faisant notamment appel à plusieurs experts en méthodologie qui n'avaient été directement associés ni à l'évaluation initiale des données probantes ni à la notation des recommandations. Au besoin, il a modifié par cette dernière évaluation la notation de valeur probante ou la catégorie attribuée à une recommandation.
Table 2.
Définitions
À une conférence de concertation tenue en 1993, on a défini l'ostéoporose comme une affection générale du squelette se caractérisant par une faible masse osseuse et une détérioration micro-architecturale du tissu osseux causant une fragilisation et des risques accrus de fracture15. À une conférence récente de concertation des National Institutes of Health aux États-Unis, on a modifié cette définition en parlant d'une affection du squelette se caractérisant par une perte de résistance des os prédisposant aux fractures. La résistance osseuse réside dans deux grandes propriétés, celles de la densité et de la qualité des os16. À l'heure actuelle, le seul indice cliniquement applicable de qualité osseuse est probablement les antécédents de fractures de fragilisation. Faute de modes de mesure de la qualité des os, le diagnostic d'ostéoporose fait généralement intervenir le facteur de densité minérale osseuse faible. (Note : l'Organisation mondiale de la santé (OMS)17 définit la fracture de fragilisation comme une fracture causée par une lésion qui ne suffirait pas à fracturer l'os dans son état normal, soit le résultat d'une perte de résistance des os à la compression et(ou) à la torsion. Cliniquement, une fracture de fragilisation peut se définir comme étant causée par un traumatisme minimal comme une chute d'une hauteur correspondant à la taille d'une personne ou moins ou encore ne s'expliquant par aucun traumatisme identifiable.)
Dans son interprétation des résultats de DMO, la SOC a voulu adopter les définitions très répandues du groupe d'étude de l'OMS18,19 et fondées sur la comparaison de la DMO du patient avec la DMO moyenne d'une population normale de jeunes adultes de même sexe et de même race. Le sujet se voit attribuer un score T, soit le nombre d'écarts types en plus ou en moins par rapport à la DMO moyenne de jeunes adultes normaux :
1. La DMO normale se définit comme un score T compris entre +2,5 et -1,0, inclusivement (elle se situe entre 2,5 écarts-types (ET) au-dessus de la moyenne des jeunes adultes et 1 ET au-dessous de cette même moyenne, inclusivement).
2. L'ostéopénie (DMO basse) correspond à un score T compris entre -1,0 et –2,5. C'est aussi un terme qu'emploient les radiologues pour indiquer que, sur un cliché radiographique ordinaire, les os semblent être déminéralisés.
3. À l'ostéoporose, on associe un score T de -2,5 ou au-dessous.
Le groupe d'étude de l'OMS a ajouté une quatrième catégorie, celle des formes sévères de l'ostéoporose pour les patients dont le score T est à – 2,5 ou au-dessous et qui ont aussi subi une fracture de fragilisation. Dans le présent document, les recommandations relatives aux facteurs de risque devraient faire très nettement ressortir l'importance des antécédents de fractures dans l'évaluation des sujets pour l'ostéoporose.
On se sert du terme «efficace» pour désigner la valeur probante d'un essai randomisé et contrôlé (ERC ou essai sur échantillon aléatoire contrôlé) et du terme «utile» pour désigner celle d'une étude d'observation non expérimentale. Le terme «périménopause» décrit une période d'évolution de plusieurs années qui comprend la préménopause et la première année qui suit l'arrêt des menstruations. Le terme «ménopause» décrit quant à lui la période d'une ou plusieurs années suivant la dernière menstruation. On s'est écarté de la terminologie antérieure sur la thérapie aux œstrogènes et à la progestine-progestérone des femmes ménopausées. Il y a environ dix ans, la SOC a adopté le terme «hormonothérapie ovarienne» (HTO) pour faire savoir que les changements hormonaux de préménopause et de ménopause ont tout d'un phénomène normal. Le CCS a maintenu cette position, mais pour que le tout soit plus compréhensible à ceux qui utiliseront les lignes directrices, on a décidé d'employer l'expression «thérapie aux œstrogènes et à la progestine-progestérone», ainsi que l'abréviation de l'hormonothérapie substitutive, à savoir «HTS».
Enfin, une recommandation de thérapie spécifique de première intention de l'ostéoporose repose sur des données probantes de niveau 1 pour la prévention des fractures de fragilisation (il s'agit surtout de fractures vertébrales), mais elle pourrait être modifiée s'il se présente d'autres circonstances atténuantes (bilan risques-avantages défavorable, par exemple). On parle de thérapie de seconde intention lorsque les données probantes sont suffisantes à des fins de prévention de la perte osseuse, mais qu'elles sont insuffisantes à des fins de prévention des fractures ou que l'étude ou son interprétation pose un certain nombre de problèmes.
Identification des sujets à risque élevé
La SOC recommande que toutes les femmes ménopausées et les hommes de plus de 50 ans fassent l'objet d'une évaluation en fonction des facteurs de risque d'ostéoporose. Le choix de facteurs de risque clés devrait aider le médecin à repérer les cas qui exigent un complément d'évaluation et d'examen pour une éventuelle intervention médicale devant atténuer les risques de fracture ostéoporotique (de fragilisation). Les principales parties du corps à surveiller sont le poignet, l'humérus, les côtes, le corps vertébral, le bassin et la hanche. Si on constate chez un sujet un risque élevé de fracture, on recommande de discuter de traitement avec lui. Mais c'est le jugement clinique et les préférences de l'intéressé qui, avec des données probantes d'essais cliniques, détermineront quel traitement s'impose, quand et sous quelle forme.
Choix des facteurs de risque à des fins cliniques
On a proposé bien des facteurs autres qu'une DMO basse comme indices de risque de fracture. Dans le cas des femmes âgées sans antécédents de fractures de la hanche, on a relié des variables comme la densité minérale osseuse, l'apport de calcium, les antécédents maternels et même la couleur des cheveux à l'incidence de telles fractures pendant un suivi de quatre ans20. La densité osseuse combinée à l'âge, les antécédents de fractures, les diverses pharmacothérapies, la perte de poids et la condition physique représentaient d'importants facteurs de prévision. Une recension de 94 études de cohortes et de 76 études cas-témoins a dégagé quelque 80 facteurs considérés comme intervenant dans les risques de fracture21. Il reste que, lorsqu'on a caractérisé l'étroitesse de leurs liens avec les fractures, on a attribué à seulement 15 % d'entre eux un rapport de risque relatif de plus de 2. Dans la plupart des cas, il s'agissait de liens avec des affections primaires comme l'hyperparathyroïdie ou avec des traitements comme la thérapie aux glucocorticoïdes. Au nombre des autres facteurs de grand intérêt, on compte le faible poids corporel, la sédentarité et le vieillissement.
La présence de facteurs de risque clés devrait alerter le médecin et lui faire constater la nécessité de pousser l'évaluation et de peut-être songer à des soins actifs comme la pharmacothérapie pour la prévention des fractures. La DMO est la variable la plus quantifiable de prévision des fractures ostéoporotiques. La DMO basse se conjugue à d'autres facteurs de risque majeurs pour accroÎtre le risque de fracture individuel. On devrait ainsi mesurer la DMO chez une femme ménopausée ou un homme de plus de 50 ans qui présente l'un de ces autres facteurs de risque majeurs de fracture.
Les facteurs de risque de fracture ostéoporotique ne doivent pas être considérés comme indépendants les uns des autres; ils sont cumulatifs, et ils doivent être examinés par rapport à des données de référence en fonction de l'âge et du sexe. Ainsi, pour une même DMO basse, une personne de 55 ans court bien moins de risques de fracture qu'une personne de 75 ans. De la même façon, si on a une DMO basse et des antécédents de fractures de fragilisation, on est bien plus à risque que si on a la même DMO basse, mais que l'on n'a encore jamais subi de fractures de fragilisation.
Les fractures ostéoporotiques surviennent le plus souvent chez les hommes et les femmes de plus de 65 ans, et l'utilité des interventions médicales pour prévenir les fractures n'a été démontrée que dans les populations où l'âge moyen est de plus de 65 ans. On sait toutefois que la plupart des thérapies actuellement homologuées de l'ostéoporose préviennent la perte osseuse ou y mettent fin lorsqu'on les emploie à l'âge de 50 ans ou peu après. Il paraÎt donc prudent de commencer à identifier les sujets à risque élevé dans leur cinquantaine si ceux-ci consentent au traitement.
Quatre facteurs de risque clés de fracture
Après avoir examiné la littérature médicale et avoir cerné l'influence d'éventuelles variables confondantes, nous avons reconnu les quatre facteurs clés suivants comme variables de prévision des fractures ostéoporotiques, à savoir une DMO basse, une fracture de fragilisation antérieure, l'âge et les antécédents familiaux d'ostéoporose. Une fois l'âge et(ou) la DMO pris en considération, d'autres facteurs fréquemment évoqués comme un poids de moins de 57 kilos, une perte pondérale depuis l'âge de 25 ans, une forte consommation de caféine et un faible apport en calcium ne constituaient pas des variables stables et indépendantes de prévision des risques de fracture.
Densité minérale osseuse
On a calculé le rapport entre la DMO et les risques de fracture dans un grand nombre d'études. La méta-analyse d'un certain nombre d'études antérieures par Marshall et coll.22 livre probablement encore la meilleure estimation dont nous puissions disposer. Il est clair que la DMO est la variable la plus immédiatement chiffrable de prévision de risques chez les sujets qui n'ont pas encore subi de fractures de fragilisation. Pour chaque écart-type au-dessous d'une valeur repère de DMO (moyenne du pic de la masse osseuse ou moyenne d'une population de référence ayant l'âge et le sexe du sujet), le risque de fracture augmente environ du double. Il faut toujours voir le risque sous l'angle de l'âge du sujet. Une personne de 25 ans ayant une DMO basse (score T de -2,5) court un très faible risque sur dix ans et celui-ci n'est guère supérieur à celui que connaÎt une personne du même âge ayant une DMO élevée. Il reste que, à DMO égale, une personne de 65 ans a un risque de fracture sur dix ans bien plus élevé qu'une personne de 25 ans.
Quels sont les facteurs de risque pour une DMO basse ou, à toutes fins utiles, qui devrait-on sélectionner pour des mesures de DMO? C'est là une question lourde de conséquences du point de vue économique. À quels critères devrait-on se reporter afin de sélectionner les gens pour une ostéodensitométrie?
Le Tableau 3 récapitule les facteurs de risque d'ostéoporose. On recommande une ostéodensitométrie chez les gens présentant au moins un facteur de risque majeur ou deux mineurs (Figure 1, Tableau 3). On a tenté à plusieurs reprises de concevoir des outils de décision pouvant aider les médecins à sélectionner les sujets pour une ostéodensitométrie23,24,25 par diverses combinaisons de facteurs de risque : âge, fractures antérieures, utilisation d'œstrogènes, arthrite rhumatoïde, tabagisme, faible poids corporel et antécédents familiaux de fracture ostéoporotique.
Table 3.
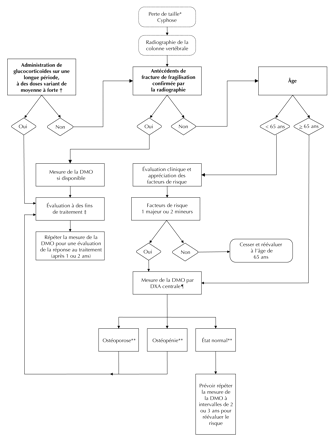
Fig. 1 : Qui devrait faire l'objet d'un examen diagnostique pour l'ostéoporose?
Notes : * Perte de taille rapportée de 4 cm; perte de taille mesurée de 2 cm [catégorie D]. †Dose variant de faible à moyenne : 2,5 à 7,5 mg de prednisone par jour; dose variant de moyenne à forte : plus de 7,5 mg de prednisone par jour. ‡Voir la figure 2. ¶DXA centrale : colonne vertébrale et hanche. ** Selon la définition de l'Organisation mondiale de la santé.
Aucun de ces instruments de décision n'est exempt de problème. En cas d'application à toute la population de femmes ménopausées de plus de 50 ans, on se trouve à sélectionner un grand nombre d'entre elles pour une ostéodensitométrie26. Toutefois, tous ces outils semblent identifier au moins 90 % des femmes de plus de 65 ans. Dans les lignes directrices de la National Osteoporosis Foundation25, on fait valoir qu'il est aussi rentable de soumettre à un examen toutes les femmes de plus de 65 ans, mais cette recommandation repose sur l'hypothèse selon laquelle les patientes recevraient à peu de frais la thérapie à l'œstrogène-progestérone.
Les études épidémiologiques démontrent amplement que l'âge est un facteur de risque majeur de fracture. Comme la DMO basse en est un autre et que la DMO diminue avec l'âge, il doit aussi y avoir un âge où il convient de commencer à recourir à l'ostéodensitométrie comme outil de dépistage. La SOC est d'avis que l'ostéodensitométrie convient en effet à un dépistage sélectif chez les gens de moins de 65 ans et à un dépistage intégral chez les femmes de 65 ans et plus à cause des risques élevés d'ostéoporose et de fracture qui se présentent alors dans la vie de ces personnes.
Fracture de fragilisation antérieure
Si on a déjà subi une fracture de fragilisation, on s'expose davantage à en connaÎtre d'autres20,27,28,29,30. Le risque est de 1,5 à 9,5 fois supérieur, selon l'âge de l'évaluation, le nombre de fractures antérieures et leurs sites anatomiques respectifs27,28,30,31,32,33,34.
Ce sont les fractures vertébrales qui ont été le mieux étudiées sous cet angle. L'existence d'une première fracture vertébrale se trouve au moins à quadrupler le risque d'une deuxième fracture35,36. L'étude du groupe placebo d'un important programme récent d'essais cliniques37 indique que 20 % des sujets qui ont eu une fracture vertébrale pendant la période d'observation en ont subi une autre dans l'année qui a suivi. Ces fractures sont aussi l'indice de risques accrus de fracture de fragilisation dans d'autres parties du corps comme la hanche38. Dans un essai clinique du risédronate38, on a rattaché la combinaison d'une fracture vertébrale et d'une DMO basse à une augmentation du double du risque (de 3 % à 6 %) de fracture de la hanche sur trois ans, chez les femmes de plus de 70 ans. De même, les fractures du poignet permettent de prévoir les fractures des vertèbres et de la hanche30. Ainsi, les sujets ayant subi une fracture de la hanche s'exposent davantage à une deuxième fracture de la hanche. Si l'on réunit les résultats de toutes les études (chez les femmes et les hommes) pour tous les sites anatomiques de fracture, on constate que les gens ayant déjà subi une fracture, peu importe le site anatomique, s'exposent 2,2 fois plus à des fractures que ceux qui n'en ont jamais subi (intervalle de confiance [IC] 1,9-2,6)30.
Âge
L'âge contribue largement au risque de fracture20,26,34,39. Selon la conclusion de Kanis et coll. dans une étude récente40, les probabilités sur dix ans de fracture de l'avant-bras, de l'humérus, de la colonne vertébrale ou de la hanche vont jusqu'à octupler chez les femmes de 45 à 85 ans et à quintupler chez les hommes (Tableau 4).
Table 4.
Antécédents familiaux de fractures ostéoporotiques
C'est dans le cas des fractures de la hanche que l'on a le mieux étudié ce facteur. Dans l'étude «The study of osteoporotic fractures»20, par exemple, on a reconnu que les antécédents maternels de fractures de la hanche représentaient un facteur de risque clé de fracture de la hanche dans une population de femmes âgées. Que la grand-mère maternelle ait subi de telles fractures accroÎt également les risques pour la descendance41.
Dans la plupart des études, on s'est attaché à la mère ou aux autres membres féminins de la famille du sujet, mais l'influence génétique sur les risques d'ostéoporose est multifactorielle. On ne devrait pas fermer les yeux sur les antécédents de fractures ostéoporotiques chez les parents masculins au premier ou au deuxième degré. Dans les études épidémiologiques, l'insistance sur les fractures ostéoporotiques chez les parents féminins du sujet tient probablement à la perception que l'ostéoporose est surtout une maladie des femmes. On sait aujourd'hui qu'elle est aussi répandue chez les hommes. Bien que les recommandations visent les fractures de la hanche qu'a pu subir la mère ou la grand-mère du sujet, il faut tenir compte des autres membres de la famille au moment d'évaluer la contribution génétique aux risques d'ostéoporose.
Le phénomène de l'influence génétique sur l'ostéoporose et la DMO importe au plus haut point. On estime en effet que l'hérédité rend compte de la variabilité de la DMO dans une proportion de 50 % à 80 %42. L'influence des gènes sur les os a fait l'objet d'importantes études scientifiques, et on a relié un certain nombre de gènes à l'ostéoporose. Les découvertes n'ont toutefois pas encore débouché sur une application clinique pour le diagnostic et le traitement de cette maladie au niveau des praticiens, aussi avons-nous choisi de ne pas réviser dans le présent document la génétique de l'ostéoporose sinon, pour insister plutôt sur l'importance que peuvent revêtir les antécédents familiaux d'ostéoporose.
Moins d'études ont porté sur les facteurs de risque de fracture ostéoporotique chez les hommes. On sait néanmoins que, comme chez les femmes, l'âge, la DMO basse et les fractures de fragilisation antérieures accroissent ce risque. Nous ne mentionnons pas les antécédents familiaux de fractures comme facteur de risque pour la population masculine, mais il ne faut pas négliger ce facteur. Nous avons relevé trois études43,44,45 consacrées aux fractures ostéoporotiques chez les hommes et dans lesquelles on livre des données probantes de niveau 1 pour les facteurs de risque d'ostéoporose, mais deux d'entre elles44,45 ne traitent pas des antécédents familiaux d'ostéoporose.
Autres facteurs de risque majeurs
Chutes
Parce que les fractures sont fréquemment associées aux chutes, on devrait prévoir dans une évaluation des risques l'examen des antécédents de chutes ou des facteurs qui augmentent les risques de tomber. Au nombre des facteurs qui entrent en jeu, on compte des indices de fragilité générale comme la diminution de force musculaire (incapacité de se lever d'une chaise sans aide), les défauts d'équilibre et le faible poids corporel20. Les pertes d'acuité visuelle rendent également les chutes plus probables20. Une étude prospective46 menée auprès d'une population ambulatoire de femmes âgées a reconnu trois facteurs significatifs de prévision des risques de fracture ultérieure de la hanche qui étaient indépendants de la DMO du fémur proximal, à savoir une démarche plus lente, une difficulté de marche talon-orteils et une perte d'acuité visuelle. Dans une étude subséquemment réalisée47 auprès du même groupe de femmes, on a constaté que l'absorptiométrie biénergétique à rayons X (DXA), l'ultrasonométrie quantitative, la vitesse de la marche et l'âge permettaient de façon équivalente de dépister les femmes à risque élevé de fracture. En combinant les diverses variables de prévision, on se trouvait à accroÎtre la sensibilité, mais non pas au point de rendre cet examen utile à un dépistage de population. Il convient de noter que les chutes causent des fractures, que le sujet souffre d'ostéoporose ou non, mais que la personne qui en est atteinte s'expose d'autant plus aux fractures qu'elle a tendance à tomber.
Utilisation de glucocorticoïdes
Une thérapie systémique aux glucocorticoïdes qui dure plus de deux ou trois mois, et ce, pour toute affection, constitue un facteur de risque majeur de perte osseuse et de fracture, plus particulièrement chez les femmes ménopausées et les hommes de plus de 50 ans48. Dans la plupart des études et des énoncés de lignes directrices, on considère une dose quotidienne de prednisone de 7,5 mg et plus (ou l'équivalent) comme seuil de déclenchement pour une évaluation et une intervention clinique destinées à prévenir ou à traiter l'ostéoporose provoquée par les glucocorticoïdes48. Il est possible de reconnaÎtre deux principaux groupes de sujets hautement exposés.
· Les sujets à qui le médecin prévoit prescrire ou a déjà prescrit une dose quotidienne de 7,5 mg et plus de prednisone, pendant plus de trois mois, devraient faire l'objet d'une évaluation en vue d'une thérapie de préservation de la masse osseuse (voir la Figure 1).
· Les sujets qui ont reçu une thérapie aux glucocorticoïdes pendant plus de trois mois à une dose journalière de moins de 7,5 mg de prednisone devraient aussi être évalués pour les risques d'ostéoporose. Ils devraient à tout le moins faire l'objet d'une ostéodensitométrie, car une posologie d'un peu plus de 2,5 mg par jour sur une longue période est liée à une aggravation des risques de fracture.
Une étude de cohorte rétrospective49 avec des données tirées de la General Practice Research Database du Royaume-Uni a permis de comparer 244 235 sujets traités à la prednisone à autant de patients appariés en fonction de l'âge, du sexe et du genre de pratique en cabinet. On a ainsi associé des doses de 2,5 à 7,5 mg par jour à un accroissement des risques de fracture. Que la prednisone ou l'affection visée par cette pharmacothérapie soit à l'origine ou non de risques accrus de fracture, la leçon que livre cette importante étude cas-témoins est que les sujets recevant plus de 2,5 mg de prednisone par jour devraient être considérés comme plus exposés et qu'un complément d'évaluation s'impose (ou du moins une ostéodensitométrie).
Autres facteurs
Une diversité d'états cliniques se trouve liée à la perte osseuse et à l'ostéoporose secondaire et les cliniciens devraient s'attarder à l'exposition de chacun de leurs patients à ces affections. Parmi celles que peut observer un omnipraticien, mentionnons l'hypogonadisme, la ménopause précoce (avant l'âge de 45 ans), l'héparinothérapie chronique, les syndromes de malabsorption, l'arthrite rhumatoïde et les antécédents d'hyperthyroïdie clinique. Les facteurs de risque énumérés au Tableau 3 devraient servir à l'évaluation des gens répondant à ces critères de risque d'ostéoporose ou de constatation de la présence de cette maladie. Le dépistage est fonction de la disponibilité d'une intervention thérapeutique éprouvée.
Déclarations sommaires
1. Quatre facteurs clés, à savoir la densité minérale osseuse (DMO) basse22, la fracture de fragilisation antérieure27,28,30,31,32,33,34, l'âge20,26,34,41 et les antécédents familiaux d'ostéoporose20,41 se distinguent comme variables de prévision des fractures liées à l'ostéoporose [niveau 1].
2. Une DMO basse devrait être considérée comme un facteur de risque majeur, mais les gens ayant subi une fracture vertébrale ou une autre fracture ostéoporotique devraient être considérés comme atteints d'ostéoporose même si leur DMO ne se situe pas dans l'intervalle des valeurs caractéristiques de cette maladie50 [niveau 1].
3. La thérapie aux glucocorticoïdes est un facteur de risque majeur d'ostéoporose et de fractures ostéoporotiques si elle dure plus de trois mois48, même à des doses qui ne sont que légèrement supérieures à 2,5 mg de prednisone par jour49 [niveau 2].
Recommandations
1. Les facteurs de risque majeurs énumérés dans le Tableau 3 permettent le mieux de prévoir l'ostéoporose chez les femmes ménopausées, mais lorsqu'ils sont applicables, ils peuvent aussi servir à une évaluation semblable chez les hommes de plus de 50 ans. Ils ont un effet cumulatif tel que, si par exemple on présente une DMO basse et une fracture de fragilisation, ou que l'on a plus de 65 ans avec une DMO se situant dans l'intervalle des valeurs caractéristiques de l'ostéoporose, on devrait être considéré comme hautement exposé à des fractures et devant recevoir une thérapie [catégorie A].
2. Les gens qui reçoivent 7,5 mg et plus de prednisone par jour pendant plus de trois mois devraient faire l'objet d'une évaluation en vue d'une thérapie de préservation de la masse osseuse [catégorie A].
3. Les gens recevant plus de 2,5 mg de prednisone par jour devraient être considérés comme plus exposés aux fractures de fragilisation et devant faire l'objet d'un complément d'évaluation ou du moins d'une ostéodensitométrie [catégorie B].
4. Les gens ayant d'autres affections ou médications que l'on sait liées à l'ostéoporose devraient être évalués pour les autres facteurs de risque; ceux qui présentent une DMO basse ou ont déjà subi des fractures de fragilisation sont des candidats à une intervention thérapeutique [catégorie D].
Diagnostic de l'ostéoporose
Par le passé, on a diagnostiqué l'ostéoporose tard dans son évolution, c'est-à-dire au moment où les os étaient affaiblis au point de pouvoir se fracturer. Si l'on se reporte à la définition que donne de cette maladie le groupe d'étude de l'OMS17, le diagnostic dans ce cas dépend aujourd'hui d'une mesure de la DMO. Cette classification est fondée sur les risques de fracture, mais les données probantes produites et donc cette classification ont été élaborées en fonction de femmes ménopausées caucasiennes. Nous nous sommes gardés de prendre position en ce qui concerne les appariements en fonction du sexe et de la race. On s'interroge toujours sur le groupe de référence à employer pour établir les scores T chez les hommes. La DMO mesurée est comparée à la DMO moyenne des jeunes adultes de même sexe et de même race.
Détection des fractures
Il est toujours possible de reconnaÎtre une ostéoporose fracturaire sur les radiographies de la colonne vertébrale, mais comme les deux tiers environ des fractures vertébrales ne sont pas diagnostiquées en clinique, on ne peut se fier uniquement aux clichés obtenus pour investiguer des dorsalgies. On ne s'entend pas encore parfaitement sur ce qui constitue une fracture vertébrale, mais le critère le plus répandu de déformation découle de mesures de la taille verticale d'une vertèbre à son extrémité antérieure, médiane (ou point central) et postérieure, sur un cliché latéral de la colonne vertébrale. Si les valeurs mesurées diffèrent de 20 % et plus les unes des autres ou de mesures analogues des vertèbres sus-jacentes ou sous-jacentes, les vertèbres en question sont considérées comme ayant une déformation fracturaire si l'on a exclu les causes congénitales, développementales, dégénératives ou autres d'une telle déformation33. Des données probantes de niveau 1 démontrent que la présence d'une de ces fractures implique un risque de récidive fracturaire correspondant au risque lié à une DMO inférieure d'un écart-type par rapport au pic de la masse osseuse. Une meilleure détection et une meilleure mesure des déformations vertébrales constituent une opportunité de choix pour augmenter la détection précoce de l'ostéoporose.
Mesure osseuse
On dispose en général de peu de bons essais prospectifs en technologie de diagnostic pour les mesures osseuses si on les compare aux essais cliniques d'intervention. La plupart des études présentées sont des études de profil transversal (niveau 2) ou de comparaison de deux techniques et plus dans des populations où prédominent habituellement les femmes ménopausées caucasiennes. Il y a peu de données sur les hommes et les autres races.
Les techniques de mesure osseuse peuvent se répartir entre les catégories de mesure du squelette central (colonne vertébrale, fémur proximal, ensemble du squelette, etc.) et celles de mesure de segments périphériques du squelette. Les mesures du squelette central se font le plus souvent par la technique de l'absorptiométrie biénergétique à rayons X (DXA). Des données probantes de niveau 1 démontrent que la mesure DXA (compte tenu de l'âge) est le mode le plus utile d'estimation des risques de fracture chez les femmes ménopausées caucasiennes22,41.
L'ultrasonométrie quantitative (QUS) a été abondamment évaluée pour l'examen densitométrique du squelette périphérique. On a soumis deux groupes de femmes, respectivement de 65 et de 75 ans et plus, à des études prospectives à grande échelle, selon les données probantes51,52 et ayant pour objet l'efficacité de l'ultrasonométrie du calcanéum. La méta-analyse de ces études53 fait voir un risque relatif de fracture de la hanche pour chaque écart-type (RR/ET) de 1,6 (IC à 95 % 1,4–1,8), alors que la mesure directe de la hanche donnait une valeur prédictive supérieure : RR/ET de 2,4. Même si la prévision du risque de fracture pour d'autres parties du corps (poignet et colonne vertébrale) procurée par l'ultrasonométrie du calcanéum est à peu de chose près la même qu'une mesure directe de DMO à ces sites52, il demeure que la mesure de la DMO à la hanche constitue la méthode préférée pour prédire le risque de fracture de la hanche.
Avant de songer à substituer l'ultrasonométrie calcanéenne à la DXA centrale, on se doit d'entreprendre de vastes études prospectives afin de démontrer si la première est au moins aussi bonne que la seconde pour la prévision des fractures chez les femmes périménopausées et ménopausées, et si un traitement fondé sur les résultats de l'ultrasonométrie calcanéenne est au moins aussi efficace. Bien qu'il y ait des données probantes de niveau 1 démontrant que la QUS fournit des mesures de densité osseuse qui peuvent être utilisées pour une estimation des risques de fracture avec une puissance semblable à celle de la DXA, toutes les études ont porté sur des populations âgées54,55.
On compte au moins six appareils commerciaux d'ultrasonométrie quantitative conçus pour la mesure de la «qualité» osseuse du calcanéum. Des études croisées montrent une bonne corrélation entre les six appareils pour le double paramètre de la vitesse du son (SOS) et de l'atténuation des ultrasons à large bande (BUA). Les coefficients de corrélation étaient significatifs à 0,73-0,93 pour le paramètre SOS et à 0,71-0,92 pour la BUA. Il demeure que les résultats obtenus avec ces divers appareils n'étaient pas interchangeables52. Pour comparer les résultats venant d'appareils ultrasonométriques différents, on devra développer des formules de normalisation par des études croisées comme lorsqu'on a comparé les valeurs de DXA centrale d'Hologic, de LUNAR et de Norland54,55.
Le suivi de la réponse au traitement de l'ostéoporose par une ultrasonométrie du calcanéum ne remplace pas une mesure directe de la colonne lombaire, du col fémoral ou de la hanche totale. La corrélation entre des changements des paramètres de BUA, de SOS et de combinaisons mathématiques des deux, appelées «rigidité», et les changements de DMO centrale était soit non significative soit trop ténue pour offrir une quelconque utilité clinique56. Cette absence d'association peut s'expliquer par au moins deux facteurs. La marge d'erreur de la précision de l'ultrasonométrie calcanéenne pourrait ne pas être assez basse pour révéler des changements de minéralisation du calcanéum sur des intervalles d'intérêt comme la période de un à trois ans qui suit le traitement. Ainsi, avec une erreur de précision de 2,3 % pour la rigidité, on doit atteindre un changement positif ou négatif de 6,4 % pour que le résultat soit jugé significatif à un niveau de confiance de 95 %. De plus, il se peut que le calcanéum ne réagisse pas au traitement comme la colonne lombaire et le fémur. On a constaté que d'autres techniques de densitométrie périphérique comme la tomodensitométrie quantitative périphérique (pQCT), la DXA calcanéenne et radiale ou l'absorptiométrie radiographique étaient discriminantes quant à la présence ou l'absence de fractures préexistantes chez les femmes ménopausées caucasiennes. Toutefois, ces études ne constituent pas des données probantes de niveau 1. Chez les hommes de toute race et les femmes ménopausées non caucasiennes, il est probable que le même rapport existe entre les valeurs d'ultrasonométrie quantitative et la présence de fractures, mais les données sont trop peu nombreuses pour qu'on puisse l'affirmer en toute certitude. Les données suggèrent qu'en combinant la mesure osseuse à d'autres moyens d'estimation des risques ou en conjuguant par permutation diverses méthodes de mesure osseuse, il est possible d'améliorer cette estimation, mais il n'y a pas encore consensus à ce sujet dans la littérature médicale.
La plus grande partie de l'expérience acquise en matière d'estimation des risques de fracture découle des mesures de la DMO obtenues par DXA axiale (centrale). Toutefois les appareils de DXA mesurant la DMO de la colonne lombaire et du fémur ne sont pas facilement accessibles dans les régions éloignées ou peu peuplées. Dans ces cas, des appareils portatifs moins chers sont disponibles, tels l'ultrasonométrie, la radiogrammétrie, l'absorptiométrie radiographique et l'absorptiométrie monophotonique (SPA), mais le lien entre la DMO basse à un site appendiculaire et l'accroissement des risques de fracture est bien moins connu pour ces techniques.
La DMO du radius mesurée par SPA permet de prévoir les fractures de fragilisation tant chez les hommes que chez les femmes57. Lors d'un suivi d'une grande population de femmes blanches âgées ayant eu une ostéodensitométrie axiale et appendiculaire de référence, on a constaté que la DMO des sites périphériques était prédictive du risque de fracture ultérieure58. Le risque relatif de fracture de la hanche ultérieure pour chaque écart-type de réduction de la DMO de cette population était le même pour le radius médian (RR 1,7) et distal (RR 1,8) et la colonne vertébrale (RR 1,7). Dans cette même étude, on a observé un risque relatif supérieur si la mesure de DMO était obtenue au calcanéum (RR 2,3) ou à la hanche (RR 3,0). Dans une autre étude59, le taux de probabilité d'une déformation vertébrale était le même pour l'absorptiométrie radiographique métacarpienne, la DXA vertébrale, la SPA radiale,la DXA calcanéenne et l'ultrasonométrie du calcanéum. Le taux de probabilité était de 1,4 à 1,9 pour chaque réduction d'un écart-type, après avoir pris en compte l'âge, et toutes les mesures procuraient des valeurs utiles quant à la probabilité de déformation vertébrale.
La propagation des ultrasons dans l'os dépend de la masse de cet os, de sa structure et de ses propriétés matérielles. La BUA mesure la variation de l'atténuation des ultrasons avec la fréquence de l'onde sonore incidente. On peut mesurer la SOS de l'os en relevant la durée de propagation des ultrasons sur une certaine distance. Des études prospectives démontrent que, chez les femmes plus âgées, les deux paramètres BUA et SOS permettent de prévoir les fractures avec une puissance semblable à celle de la DXA60,61.
La radiogrammétrie est la mesure géométrique des dimensions osseuses par la radiographie de haute résolution. L'avènement récent de l'analyse par ordinateur d'images radiographiques numérisées est venu accroÎtre la précision de cette technique, la rendant comparable à cet égard à la technique DXA, d'où un rôle diagnostique possible pour cette technique lorsqu'on ne peut disposer d'un appareil DXA. Les résultats radiogrammétriques sont en corrélation avec les résultats DXA tant axiaux qu'appendiculaires62. La radiogrammétrie procure, pour la DMO et les risques de fracture, des données transversales semblables à celles obtenues par la SPA et la tomodensitométrie quantitative63. Cependant il n'y a pas de données liant les résultats de radiogrammétrie informatisée à l'estimation des risques de fracture.
La DMO mesurée par absorptiométrie radiographique des phalanges est en corrélation avec la DMO de l'avant-bras distal, ainsi qu'avec la DMO de la colonne lombaire et du fémur proximal64.
Au cours du traitement de l'ostéoporose, les changements de DMO axiales et appendiculaires ne sont pas en relation étroite avec les changements de risque de fracture65. Le léger gain de DMO observé ne rend compte que d'une fraction de la diminution du risque de fracture induite par une thérapie antirésorptive.
Précision et mesures répétées
L'évaluation des changements de la DMO dans le temps établit le taux de la perte osseuse (en distinguant les cas de perte rapide et de perte lente) et confirme une réponse positive au traitement. Toutefois, le taux annuel moyen de perte osseuse chez les femmes ménopausées est de 0,5 % à 2 % et la plupart des traitements font augmenter la DMO de 1 % à 6 % en trois ans. Comme les variations sont relativement modestes, seul un examen très précis permettra de constater les changements à court terme. Il faut bien comprendre ce qu'est l'interprétation des mesures répétées et les principes statistiques de cette interprétation pour juger si un changement offre un intérêt clinique et pour ne pas assimiler par mégarde des variations dues au hasard à des changements bien réels. À son tour, cette compréhension aidera à établir l'intervalle temporel à prévoir entre les mesures pour permettre une évaluation juste de la réponse au traitement ou de la progression de la maladie.
Les facteurs humains (chez l'opérateur comme chez le sujet) plutôt que l'instrumentation constituent d'ordinaire la source majeure de variation. Grâce à un programme de contrôle de la qualité par lequel on contrôlera le rendement tant de l'opérateur que de l'appareillage, on s'assurera que les examens sont optimaux et qu'une procédure appropriée a été appliquée66,67,68.
On a décrit des techniques pour une comparaison des résultats obtenus avec des appareils et des fournisseurs différents. Bien que les résultats DXA tirés d'appareils différents soient en étroite corrélation, les méthodes sont trop imprécises pour pouvoir s'appliquer aux sujets individuels et continuent à se prêter au mieux à des comparaisons de groupes comme dans des essais cliniques54,55. Les résultats d'appareils DXA de modèle identique et en provenance d'un même fournisseur peuvent accuser des différences significatives d'étalonnage. Même après un interétalonnage, l'erreur de précision par l'emploi d'appareils différents est supérieure à celle que l'on obtient par l'emploi d'un appareil unique69. On devrait donc utiliser le même appareil pour les mesures de base et de suivi.
On s'interroge quelque peu sur la façon d'exprimer les changements de mesure et leur interprétation. On peut exprimer un changement comme une différence absolue (g/cm2 pour la DXA) ou une différence relative (%) de la DMO. L'expression en valeur relative est la plus courante. Les données probantes indiquent que l'erreur observée sur les valeurs absolues est aussi grande (sinon plus grande) chez les patients âgés et ceux atteints d'ostéoporose que chez les jeunes patients normaux et qu'il faut prendre la différence absolue de mesures exprimées en g/cm2 plutôt que la différence relative en pourcentage pour juger du caractère significatif des résultats70. L'environnement clinique, les caractéristiques des patients, le site de mesure et le modèle de l'appareil influencent la précision des mesures. Lorsqu'on étudie de jeunes sujets ayant une DMO normale dans un environnement de recherche, la variabilité à court terme de la DMO de la colonne lombaire mesurée par DXA est d'environ 1 %. Dans une population plus âgée, à forte prévalence de maladie et d'ostéoporose sous-jacente, elle peut même atteindre 1,7 %71. La variabilité à long terme est plus grande (2 % à 3 %) et cette valeur s'accroÎt dans un environnement de soins cliniques. La variabilité est plus marquée pour le col fémoral (jusqu'à 3,2 %) que pour la hanche totale (jusqu'à 2,5 %)72. Il ne suffit pas d'accepter les estimations nominales de précision venant des fournisseurs, car elles sont habituellement établies dans des conditions optimales et il y a normalement sous-estimation de l'erreur que l'on observe en milieu clinique. Chaque laboratoire d'ostéodensitométrie devrait établir ses propres valeurs de précision de mesure pour chaque site couramment évalué dans une population clinique type et en faire son cadre de référence pour l'interprétation des changements. Les méthodes normalisées de calcul de précision sont bien décrites73,74. Elles devraient être familières au laboratoire d'ostéodensitométrie.
DMO et risque de fracture chez les hommes
Les données sur le rapport entre la DMO et le risque de fracture chez les hommes demeurent insuffisantes. Il y a quelques études prospectives75 selon lesquelles les hommes subiraient des fractures à des valeurs de DMO supérieures à celles des femmes; d'autres76,77 disent en revanche que le rapport DMO-risque de fracture est le même pour les deux sexes. Nous avons besoin de données d'études prospectives à grande échelle pour comprendre ce rapport dans la population masculine. Le risque de fracture dépend non seulement de la DMO, mais aussi de facteurs comme les probabilités de chute et la grosseur et la géométrie des os. Les os sont plus gros chez les hommes que chez les femmes même après correction pour la taille et le poids des sujets78. Le modèle de perte osseuse en fonction de l'âge diffère aussi dans le cas des hommes. L'amincissement endocortical s'accentue avec l'âge chez les femmes, mais ce n'est pas le cas chez les hommes79, et ceci influence également la résistance osseuse. Le rapport entre la DMO et le risque de fracture pourrait également être différent chez les hommes, puisque la grosseur des os introduit un artéfact dans les valeurs de DMO de surface (il s'agit de la valeur de la densité minérale osseuse divisée par la surface osseuse mesurée, ce qui correspond à la mesure de DXA actuelle). La technique DXA se trouve à surestimer la DMO des hommes par rapport à celle des femmes. Voilà pourquoi la valeur de DMO de surface que l'on obtient par l'appareillage DXA pourrait mieux se prêter à l'évaluation du risque de fracture chez les hommes, puisque les os masculins plus gros pourraient procurer aux hommes un plus grand avantage biomécanique par rapport aux femmes.
Comme le risque à vie de fracture de fragilisation après l'âge de 50 ans est d'environ 13 % chez les hommes75, on peut l'estimer au mieux à l'aide des données de référence d'une base de données sur les hommes. Ceci est en cours actuellement partout au Canada. En utilisant les données masculines de référence, si nous mesurons la DMO par une ostéodensitométrie DXA de la hanche, de la colonne vertébrale et du radius et que nous utilisons la valeur la plus basse pour établir le diagnostic, soit un score T au-dessous de -2,5, on a constaté que la population masculine de plus de 50 ans était atteinte d'ostéoporose dans une proportion approximative de 19 %75.
Il y a encore moins de données sur le rapport DMO-risque de fracture dans la population non caucasienne, mais il apparaÎt que, à DMO égale, les hommes s'exposent autant que les femmes à des fractures80,81. On sait que les Américains d'origine asiatique ont une DMO inférieure à celle des Caucasiens, mais qu'ils présentent aussi des proportions inférieures de fractures de la hanche82. Toutefois, lorsqu'on apporte une correction en fonction des différences de taille du squelette, leurs valeurs apparentes de DMO sont en réalité supérieures à celles des femmes blanches, ce qui s'accorde avec les proportions inférieures de fractures de la hanche que l'on note. En raison de l'insuffisance des données, on n'a pas encore établi de valeurs de démarcation appropriées à des fins de diagnostic.
Les Figures 1 and 2 décrivent ceux et celles qui devraient être examinés et traités. La perte de taille significative, la cyphose, les antécédents personnels de fractures de fragilisation après l'âge de 40 ans, une prise prolongée de glucocorticoïdes, la présence de facteurs de risque cliniques et un âge de 65 ans et plus (voir Tableau 3) seraient autant d'incitatifs à prescrire une ostéodensitométrie, une radiographie de la colonne vertébrale ou les deux. On se doit d'assimiler à une fracture vertébrale une diminution non traumatique de 20 % à 25 % de la hauteur des vertèbres33.
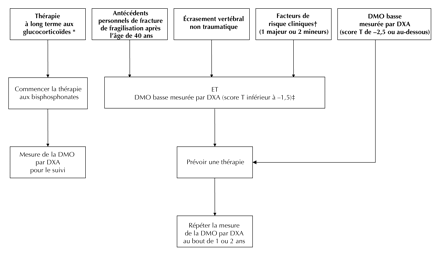
Fig. 2 : Qui devrait faire l'objet d'une évaluation des risques de fracture et être traité pour l'ostéoporose?
Notes : * ≥ 7,5 mg de prednisone pendant plus de 3 mois. †Voir le Tableau 3. ‡Nous avons choisi arbitrairement un score T inférieur à –1,5; un écrasement vertébral non traumatique [catégorie A] 117 ; des antécédents personnels de fracture de fragilisation après l'âge de 40 ans [catégorie D]; facteurs de risque cliniques [catégorie D].
Nous recommandons les examens de laboratoire suivants pour tous les sujets atteints d'ostéoporose afin d'exclure les causes secondaires : formule sanguine complète, calcium sérique, phosphatases alcalines sériques totales, créatinine sérique et électrophorèse des protéines sériques. Les lignes directrices de pratique clinique de 1996 de la SOC pour le diagnostic et le traitement de l'ostéoporose traitent plus en détail de ces examens11. Si l'on soupçonne en clinique l'existence d'autres causes secondaires, on pourra juger du besoin de pousser l'investigation.
Déclarations sommaires
4. L'absorptiométrie biénergétique à rayons X (DXA) est la méthode la plus étudiée d'estimation des risques de fracture chez les femmes. C'est le meilleur instrument à notre disposition pour l'évaluation des risques22,80 [niveau 1]. Les données sont convergentes et suffisantes pour que nous recommandions la DXA centrale en dépistage sélectif.
5. Les données dont nous disposons ne justifient pas le dépistage intégral auprès de toutes les femmes ménopausées ni chez tous les hommes de plus de 50 ans, mais une ostéodensitométrie chez les hommes et les femmes de plus de 65 ans est justifiée compte tenu de l'accroissement des risques de fracture après cet âge25 [niveau 3].
6. Toutes les techniques d'ostéodensitométrie permettent de prévoir les risques qui s'attachent à toutes les fractures de fragilisation22,40,41,51,52 [niveau 1].
7. Le meilleur élément de prévision du risque relatif de fracture du fémur proximal est la mesure de la DMO à ce site22,53 [niveau 1].
8. Une évaluation clinique combinée à une ostéodensitométrie surpasse toute méthode unique d'évaluation des risques; l'âge, la DMO et la(les) fracture(s) préexistante(s) sont les meilleurs indicateurs de risque20,21,26,30,39 [niveau 1].
9. L'indicateur le plus juste de la DMO est la mesure même de la DMO. L'«ostéopénie» détectée sur les radiographies du squelette ou les facteurs de risque d'une DMO basse ne permettent pas de bien prévoir la DMO21,26 [niveau 1]. Les outils actuels de décision sont utiles à une mise en évidence des facteurs de risque de DMO basse, mais ils ne sauraient se substituer à l'ostéodensitométrie. La décision de mesurer la DMO devrait être fondée sur les risques en fonction de l'âge, la présence d'autres facteurs de risque de fracture et une consultation avec le patient [consensus]. On devrait mesurer la DMO seulement si elle aura une influence sur les décisions de prise en charge ou de traitement.
10. Puisque les fractures de la colonne vertébrale et de la hanche sont les fractures de fragilisation consécutives à l'ostéoporose qui s'avèrent les plus importantes cliniquement, et que la DXA est celle qui mesure le mieux les os de la colonne vertébrale et de la hanche pour les risques de fracture, la DXA reste pour le moment la technologie optimale d'évaluation des risques22,40,41,53 [niveau 1].
11. On peut recourir à la DXA pour l'évaluation des sites qui répondent à la thérapie83,84,85,86 [niveau 1].
12. La justification de l'utilisation clinique de la DXA présuppose une compréhension claire de son application, la nécessité d'un contrôle de la qualité et une détermination soignée de la DMO avec une précision permettant de bien faire voir les changements les plus faiblement significatifs67,69,70,71,72,73,74 [niveau 4].
13. L'ultrasonométrie quantitative du calcanéum (QUS) semble utile à l'estimation des risques de fracture chez les femmes ménopausées de plus de 65 ans52,59,60,61 [niveau 1]. On dispose de peu de données sur son application aux hommes et aux femmes plus jeunes. Les données ultrasonométriques semblent être plus spécifiques aux appareils employés que les données DXA52,59,60,61.
14. L'ultrasonométrie quantitative du calcanéum n'est pas assez précise pour permettre un suivi à des intervalles qui soient utiles cliniquement56 [niveau 1].
15. D'autres techniques de mesure osseuse (radiogrammétrie, absorptiométrie radiographique, ultrasonométrie quantitative, etc.) peuvent avoir une valeur particulière dans l'évaluation des risques (mais non pas pour le suivi) là où les facteurs géographiques et la taille des populations restreignent la disponibilité des appareils DXA. Il n'y a toutefois pas de données probantes de niveau 1 pour permettre la généralisation de leur emploi [consensus].
16. Les incertitudes au sujet de la définition de la fracture vertébrale et la variation marquée du rendement de l'observateur dans ce contexte expliquent la majeure partie de la variabilité des résultats, notamment dans les études transversales33 [consensus].
17. La consistance dans la mesure, la détection et la description des fractures vertébrales ouvre une opportunité dans l'évaluation du risque fracturaire relié à l'ostéoporose [consensus].
18. Les données probantes sont minces quant au recours à la mesure osseuse chez les hommes, et chez les femmes non caucasiennes. Les données existantes ne contredisent pas les inférences déjà dégagées [consensus].
Recommandations
5. Nous recommandons des stratégies de dépistage sélectif des cas à risque accru (avec au moins un facteur de risque majeur ou deux facteurs de risque mineurs), ainsi qu'une mesure de la DMO par DXA centrale pour toutes les personnes âgées de 65 ans et plus [catégorie A].
6. La DXA centrale (de la hanche et de la colonne vertébrale) demeure l'outil le plus juste pour l'évaluation de la DMO en milieu clinique. L'accès aux mesures de DMO ne devrait pas être limité par les outils de décision fondés sur des facteurs de risque cliniques [catégorie A].
7. Le suivi des patients devrait être fait par DXA centrale (hanche totale et colonne vertébrale) en milieu clinique, un à deux ans après le début de la thérapie [catégorie A].
8. L'ultrasonométrie quantitative peut être envisagée pour le diagnostic de l'ostéoporose, mais non pour le suivi, du moins pour le moment [catégorie C].
9. Une perte de taille de plus de 2 cm sur un an ou une perte de taille de plus de 4 cm à l'histoire, devrait être suivie d'une radiographie de la colonne dorsolombaire à la recherche de fractures vertébrales [catégorie D].
Rôle des marqueurs biochimiques du remodelage osseux
Le remodelage osseux est un processus normal et naturel qui maintient la résistance du squelette, permet de réparer les microfractures et se révèle essentiel à l'homéostasie calcique. Au cours du processus de remodelage osseux, les ostéoblastes synthétisent un certain nombre de cytokines, de peptides et de facteurs de croissance, qui sont libérés dans la circulation. Leur concentration reflète donc le taux de formation osseuse. Les marqueurs de la formation osseuse sont notamment l'ostéocalcine sérique, les phosphatases alcalines osseuses spécifiques et le propeptide carboxyterminal du procollagène de type I (PICP).
Les ostéoclastes produisent des produits de dégradation osseuse qui sont aussi libérés dans la circulation et éventuellement éliminés par le rein. Mentionnons entre autres les peptides de liaison du collagène et les pyridinolines, que l'on peut mesurer dans le sang ou l'urine et qui permettent une estimation du taux de résorption osseuse. Au nombre des marqueurs de la résorption osseuse, on compte l'hydroxyproline urinaire, la pyridinoline urinaire (PYR), la désoxypyridinoline urinaire(D-PYR), ainsi que les télopeptides de liaison N (NTX) et C du collagène de Type I (CTX).
Les marqueurs de la formation et de la résorption osseuses peuvent servir à l'estimation des taux de remodelage osseux. Grâce à ces marqueurs biochimiques, on peut reconnaÎtre les cas de pertes osseuses rapides87. Nombre d'études transversales88,89 ont démontré que les taux de remodelage osseux, évalués par les marqueurs, s'élèvent à la ménopause et demeurent élevés. Le taux de remodelage osseux chez les femmes ménopausées est en corrélation négative avec la DMO90.
La plupart des études prospectives où l'on a évalué le rapport entre le remodelage osseux et les taux de perte osseuse étaient à court terme, et elles étaient limitées par l'erreur de précision de l'ostéodensitomètre91,92,93,94,95. L'utilité des marqueurs osseux pour identifier les cas de perte osseuse rapide a été évaluée de façon prospective sur quatre ans, dans une grande cohorte de femmes ménopausées en bonne santé87. Des concentrations plus élevées de marqueurs de la formation et de la résorption osseuses étaient en corrélation significative avec une perte osseuse accélérée et accentuée.
Dans les études de populations, il semble que les marqueurs de la résorption osseuse pourraient être des éléments utiles de prévision des risques de fracture et de perte osseuse. Des concentrations élevées de ces marqueurs pourraient être liées à des risques accrus de fracture chez les femmes âgées96,97, bien que les données en question demeurent hétérogènes. L'association entre les marqueurs de la résorption et les risques de fracture de la hanche est indépendante de la DMO, mais une DMO basse combinée à une concentration élevée de marqueurs de la résorption osseuse double le risque associé à l'un ou l'autre de ces facteurs pris isolément96. Toutefois, la valeur prédictive des marqueurs osseux dans l'évaluation individuelle des patients n'a pas encore été confirmée91. De plus, les marqueurs osseux sont actuellement limités par leur haute variabilité interindividuelle97.
Dans les essais cliniques, les marqueurs osseux peuvent être utiles pour la prévision et le suivi de la réponse thérapeutique à une thérapie antirésorptive puissante. De façon prospective, on a constaté une normalisation des marqueurs de la formation et de la résorption osseuses à la suite d'une thérapie anti-résorptive92,98,99. Une réduction de ces marqueurs semble être en corrélation avec une diminution de l'incidence des fractures vertébrales99 dans un certain nombre d'études, mais ce n'est pas nécessairement toujours le cas.
Une faible corrélation inverse de la DMO et du NTX a été observée chez les hommes100. D'autres études indiquent une piètre corrélation entre les marqueurs de la résorption osseuse et la DMO. Ainsi, la situation est moins claire dans le cas des hommes, et il faudrait plus d'essais cliniques à grande échelle.
Déclarations sommaires
19. Les marqueurs du remodelage osseux semblent utiles à l'évaluation des risques de fracture chez les femmes ménopausées âgées dans le cadre des études de populations96 [niveau 2]. De nouvelles études avec issues sur les fractures sont nécessaires pour vérifier l'utilité de ces marqueurs dans une évaluation individuelle de sujets. Les marqueurs du remodelage osseux ont peut-être un rôle futur dans la prise en charge clinique de l'ostéoporose.
20. Dans les études de populations, la combinaison d'une DMO basse et d'une concentration élevée de marqueurs du remodelage osseux pourrait fournir des indices de risque de fracture supérieurs à la DMO ou aux marqueurs du remodelage osseux lorsqu'ils sont pris isolément96 [niveau 2].
Recommandations
10. Il serait prématuré d'utiliser les marqueurs du remodelage osseux dans la prise en charge clinique courante. Il faudra que de nouvelles études confirment leur intérêt pour l'évaluation individuelle des patients. Il demeure qu'avec un raffinement des techniques de dosage et une meilleure compréhension de la variabilité biologique, nous croyons que ceux-ci deviendront un complément utile à nos moyens d'évaluation des risques et de prise en charge [catégorie B].
Prévention et traitement de l'ostéoporose
Interventions pharmacologiques
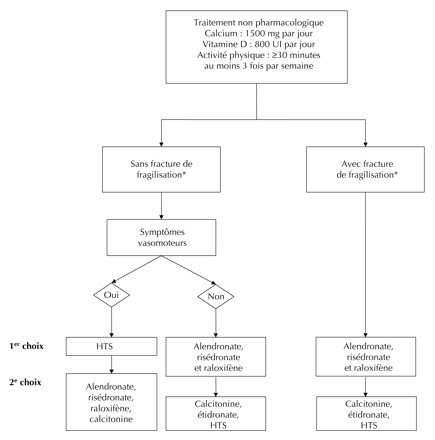
Comme l'ostéoporose est une affection multifactorielle, sa prévention et sa prise en charge sont complexes. Depuis la prévention jusqu'au traitement de la maladie fracturaire, le but est d'intervenir le plus tôt possible pour préserver la masse osseuse et l'intégrité structurale du squelette, et ainsi prévenir les fractures de fragilisation.
Les résultats d'importants essais randomisés contrôlés (ERC) prospectifs depuis dix ans nous ont aidés à délimiter les possibilités thérapeutiques, éventail qui comprend des interventions non pharmacologiques recommandées pour l'ensemble des sujets. À l'heure actuelle, les pharmacothérapies disponibles sont toutes à action antirésorptive et mettent l'accent sur une diminution du remodelage osseux. On a démontré qu'elles réduisent les risques de subir un certain nombre de fractures, mais pas nécessairement toutes. On étudie actuellement des thérapies plus récentes qui visent à accroÎtre la formation osseuse, et dont les résultats devraient être disponibles sous peu. Il est difficile d'évaluer l'efficacité antifracturaire relative des diverses thérapies, celles-ci n'ayant pas fait l'objet d'une comparaison directe dans des essais cliniques.
Bisphosphonates
Plusieurs agents antirésorptifs ont été utilisés avec succès dans le traitement de l'ostéoporose postménopausique. Toutefois, les essais cliniques récents sur les bisphosphonates fournissent invariablement la meilleure preuve d'efficacité aux fins de la prévention des fractures vertébrales et non vertébrales. Les bisphosphonates sont des analogues stables du pyrophosphate présent à l'état naturel. Ils contiennent deux groupes phosphatés liés à un atome unique de carbone dans une structure P-C-P. C'est une structure qui les rend chimiquement stables et qui est à l'origine de l'étroite affinité des bisphosphonates pour le tissu osseux101.
Les bisphosphonates inhibent la résorption osseuse par leurs effets sur les ostéoclastes102. Ils interfèrent avec le recrutement, la différenciation et l'action des ostéoclastes et ils favorisent leur apoptose102. On peut les classifier dans deux groupes selon leur mode d'action : ceux qui ressemblent le plus au pyrophosphate (comme le clodronate et l'étidronate) peuvent s'incorporer à des analogues cytotoxiques de l'adénosine-triphosphate (ATP); les bisphosphonates azotés plus puissants (alendronate et risédronate) provoquent l'apoptose des ostéoclastes en interférant avec la prénylation des protéines par leurs effets sur la voie du mévalonate et donc sur la circulation intracellulaire de protéines régulatrices clés. Ces deux mécanismes d'action peuvent aider à expliquer certaines des différences pharmacologiques entre les deux catégories de bisphosphonates.
À l'heure actuelle, les bisphosphonates homologués pour le traitement de l'ostéoporose au Canada sont l'étidronate, l'alendronate et le risédronate. Certes ce sont tous des bisphosphonates, mais ils varient considérablement dans leur puissance, leur capacité d'inhiber la résorption osseuse, leur toxicité et leur schéma posologique. L'absorption orale des bisphosphonates est médiocre (1 % à 5 % seulement), même lorsque pris dans un estomac vide. Leur demi-vie plasmatique est d'une heure et leur taux de clairance rénale varie de 40 % à 80 %. Le reste est absorbé par le tissu osseux où sa demi-vie est longue. L'effet secondaire le plus courant des bisphosphonates est le dérèglement gastro-intestinal, lequel est souvent lié à la posologie.
Étidronate : L'étidronate est le premier bisphosphonate dont on ait démontré l'utilité dans le traitement de l'ostéoporose103,104,105,106,107,108,109,110,111,112,113. Il est généralement bien toléré par l'organisme. On signale peu de cas de dérèglement gastro-intestinal, la diarrhée étant le trouble le plus fréquent. En administration continue sur une longue période, cette substance peut nuire à la minéralisation osseuse et produire de l'ostéomalacie. C'est la raison pour laquelle on l'administre sur un mode intermittent, d'ordinaire à raison de 400 mg par jour sur deux semaines une fois aux trois mois.
Dans deux ERC111,113, on a examiné l'efficacité antifracturaire de l'étidronate cyclique chez les femmes ménopausées ayant des fractures vertébrales préexistantes. Dans chaque étude, l'étidronate a largement augmenté la DMO de la colonne lombaire et il a diminué de façon inégale les taux de fractures vertébrales. Ces études indiquent que l'étidronate a un certain effet sur la prévention de nouvelles fractures vertébrales chez les femmes ménopausées présentant une ostéoporose sévère. Rien n'indique que l'étidronate ait un effet bénéfique sur les risques de fracture de la hanche ou de fracture non vertébrale.
Alendronate : L'alendronate est un bisphosphonate azoté qui, en administration continue à raison de 5 mg par jour, prévient l'ostéoporose et, à une dose de 10 mg par jour, permet de traiter une ostéoporose confirmée. Récemment, on a démontré qu'une dose hebdomadaire de 70 mg avait un effet comparable sur la DMO à une dose quotidienne de 10 mg114. L'alendronate est généralement bien toléré par l'organisme, bien qu'on ait signalé de rares cas d'œsophagite115.
Cette substance a amplement été étudiée pour le traitement de l'ostéoporose84,85,86,114,116,117,118,119,120,121,122,123,124,125,126,127,128,129,130,131,132. Dans une première étude de trois ans, l'alendronate a nettement diminué l'incidence de nouvelles fractures85. Depuis lors, on a examiné son efficacité dans deux grandes populations de femmes ménopausées, l'une avec fracture vertébrale préexistante et l'autre sans fracture vertébrale117,118. Chez les femmes avec fracture vertébrale préexistante, le traitement à l'alendronate a réduit d'environ la moitié l'incidence des fractures de la colonne vertébrale, de la hanche et du poignet sur une période de 3 ans. Le risque de fractures vertébrales multiples a été réduit quant à lui de 90 %. Ce fût le premier ERC à démontrer une réduction des fractures de la hanche chez les femmes atteintes d'ostéoporose ayant un apport maximal de calcium et de vitamine D. Dans une analyse rétrospective133, on a fait la preuve d'une réduction de l'incidence des fractures vertébrales cliniques après une seule année dans l'étude.
On a aussi examiné l'efficacité antifracturaire de l'alendronate chez les femmes ménopausées sans fracture vertébrale antérieure118. L'alendronate a augmenté la DMO à tous les sites mesurés et il a abaissé de façon nette (36 %) l'incidence de fracture vertébrale clinique chez les femmes dont le score T initial était inférieur à -2,5. Le «Fosamax International Trial Study Group» (FOSIT)127 a démontré, sur une période d'un an, une diminution de l'incidence des fractures non vertébrales chez les femmes ménopausées ayant un score T inférieur à -2,0. L'alendronate prévient la perte osseuse chez les femmes ménopausées normales, mais son efficacité antifracturaire dans ce contexte n'a pas été prouvée.
En résumé, l'alendronate prévient les fractures de la hanche, les fractures vertébrales, ainsi que les fractures non vertébrales chez les femmes ménopausées. L'alendronate augmente de façon invariable la DMO à tous les sites anatomiques mesurés. On l'a administré à des sujets qui prenaient aussi des œstrogènes ou du raloxifène, produisant un effet additif sur la DMO, mais aucun avantage antifracturaire n'a été démontré124.
Risédronate : Le risédronate est généralement bien toléré par l'organisme. On a rapporté occasionnellement des maux de tête et des diarrhées comme effets secondaires. Maintes études ont fait la preuve de son efficacité en administration tant quotidienne qu'hebdomadaire38,83,134,135,136,137,138. Récemment, deux grands ERC multicentres d'une durée de trois ans136,137 ont permis d'évaluer son efficacité dans le traitement de l'ostéoporose postménopausique. Après trois ans de traitement à raison de 5 mg par jour, le risédronate a diminué l'incidence des fractures vertébrales dans une proportion de 41 % et 49 %, et des fractures non vertébrales dans une proportion de 39 % et 33 %. Dans une analyse prédéterminée, on a montré qu'un traitement de risédronate à une dose de 5 mg par jour avait pour effet de réduire l'incidence des fractures vertébrales dans une proportion de 61 % et 65 % pendant la première année de thérapie. On n'a pas constaté de différences significatives pour les effets indésirables entre le groupe «risédronate» et le groupe «placebo».
Dans un grand ERC38 visant à établir l'efficacité du risédronate dans la prévention des fractures de la hanche, on a démontré que le risédronate réduisait de 40% l'incidence des fractures de la hanche chez les sujets ayant une DMO basse au col fémoral. Parmi ces dernières, chez celles qui avaient déjà subi des fractures vertébrales, le risédronate a réduit de 60 % le nombre de fractures de la hanche. Il n'y a pas eu de diminution significative des risques de fractures de la hanche chez les femmes âgées sélectionnées sur la base de facteurs de risque autres qu'une DMO basse.
En résumé, s'il est administré à raison de 5 mg par jour sur une période de trois ans, le risédronate est bien toléré par l'organisme et il réduit l'incidence des fractures vertébrales et non vertébrales chez les femmes présentant une ostéoporose postménopausique confirmée. Ajoutons que ces études ont été les premières à montrer une baisse significative de l'incidence des fractures vertébrales (fractures cliniques et subcliniques) dans la première année de thérapie.
On retrouvera dans Hodsman et coll.139 une évaluation détaillée des données probantes recueillies à ce jour sur l'efficacité de ces bisphosphonates.
Thérapie combinée : On a combiné l'administration d'étidronate cyclique à l'œstrogénothérapie chez des femmes ménopausées140,141. Dans une étude sur échantillon aléatoire141 d'une durée de quatre ans, cette thérapie combinée a produit un accroissement de la DMO supérieur à ce que pouvaient produire à eux seuls les œstrogènes ou l'étidronate. Chez les sujets traités seulement aux œstrogènes ou à l'étidronate, la DMO de la colonne vertébrale et de la hanche avait augmenté de façon moins marquée.
On a étudié les effets conjugués de l'alendronate et des œstrogènes chez des femmes ménopausées ayant reçu au préalable une œstrogénothérapie sur une période d'au moins un an124. À l'aide d'une répartition aléatoire, ces femmes ont reçu soit de l'alendronate, 10 mg par jour, soit un placebo. Au bout de 12 mois, les patientes qui prenaient à la fois de l'alendronate et des œstrogènes ont présenté une augmentation significativement supérieure de leurs DMO à la colonne lombaire et au trochanter, mais il a été impossible de tirer des conclusions sur la réduction des taux de fractures.
Les données de cet essai clinique ont été corroborées par un autre essai clinique, cette fois-ci sur une période de deux ans, et s'adressant à des femmes ménopausées, assignées de façon aléatoire à recevoir un placebo, de l'alendronate 10 mg par jour, des œstrogènes conjugués ou des œstrogènes conjugués et de l'alendronate121. Dans le groupe «placebo», la DMO de la colonne lombaire est demeuré stable pendant les deux ans. Les groupes «alendronate» et «œstrogènes conjugués» présentaient des gains semblables de DMO, alors que le groupe recevant l'alendronate et les œstrogènes conjugués avait fait un gain significativement supérieur à ceux des groupes recevant uniquement l'un ou l'autre. Ces résultats semblent indiquer que, chez les femmes qui initient une thérapie, la combinaison d'alendronate et d'œstrogènes est plus utile qu'un traitement avec l'un ou l'autre pris isolément. On a certes constaté un gain de DMO avec la combinaison, mais sans obtenir de données probantes directes sur la réduction des taux de fractures.
Traitement aux bisphosphonates chez les hommes : Il n'y a pas de données d'ERC sur les avantages d'un traitement à l'étidronate chez les hommes. Une étude a évalué l'efficacité de l'alendronate dans le traitement de l'ostéoporose masculine. Cette étude a démontré un accroissement significatif de la DMO142, et une diminution du nombre de fractures vertébrales. Dans une grande étude consacrée à l'administration de risédronate chez des hommes traités aux glucocorticoïdes, on a pu démontré une diminution significative du nombre de fractures vertébrales après un an143.
Bisphosphonates et ostéoporose induite par les glucocorticoïdes : Les études portant sur l'ostéoporose induite par les glucocorticoïdes visent deux groupes, à savoir les gens qui commencent une thérapie préventive au tout début de l'administration de glucocorticoïdes et ceux qui reçoivent une thérapie chronique aux glucocorticoïdes et qui requièrent un traitement de l'ostéoporose. Les indices abondent selon lesquels la thérapie à l'étidronate maintient la DMO des patients prenant des glucocorticoïdes144,145,146,147,148,149,150,151,152,153,154,155,156. Lorsqu'il est donné au tout début de la thérapie aux glucocorticoïdes, l'étidronate augmente légèrement la DMO de la colonne lombaire, alors qu'on observe une perte osseuse dans le groupe placebo144,145,147,149,151. Dans une étude144, on a suggéré que l'étidronate pourrait être utile en prévention des fractures vertébrales. Des ERC sur deux ans146,149 portant sur les vertus de l'étidronate pour les sujets traités à long terme par des glucocorticoïdes, ont démontré des gains de DMO. Ces résultats indiquent que l'étidronate est utile à la prévention et au traitement de la perte osseuse induite par les glucocorticoïdes et qu'il est susceptible de réduire les risques de fracture chez les femmes ménopausées traitées aux glucocorticoïdes.
On a aussi étudié l'alendronate chez des sujets traités aux glucocorticoïdes157,158,159 et chez des sujets souffrant d'un syndrome de Cushing160. On a constaté un gain statistiquement significatif de DMO à la colonne vertébrale, au trochanter et au col fémoral à des doses de 5 et 10 mg par jour. Tous les groupes ont bénéficié de la prise d'alendronate, soit les hommes, les femmes préménopausées et les femmes ménopausées. Chez les femmes ménopausées recevant une HTS, l'alendronate ajoutait un gain additionnel158; l'alendronate s'est avéré utile pour prévenir et traiter l'ostéoporose induite par les glucocorticoïdes et réduire les risques de fracture vertébrale159.
Le risédronate a été évalué dans la prévention et le traitement de l'ostéoporose induite par les glucocorticoïdes161,162,163. Par rapport au groupe placebo, on a relevé des différences significatives de DMO à la colonne lombaire et à la hanche. L'analyse des données groupées de ces études a révélé une diminution significative de l'incidence des fractures vertébrales chez les sujets prenant quotidiennement 5 mg de risédronate163.
On devrait considérer les nouveaux bisphosphonates azotés, tels l'alendronate et le risédronate, comme thérapie de première intention pour des femmes ménopausées souffrant d'ostéoporose confirmée et qui sont à haut risque de fractures. On dispose de données probantes solides démontrant leur effet sur prévention des fractures vertébrales et non vertébrales incluant les fractures de la hanche. Les bisphosphonates sont les seules thérapies qui ont démontré, par des données probantes, qu'elles peuvent réduire le nombre de fractures vertébrales consécutives à l'ostéoporose induite par les glucocorticoïdes.
Les bisphosphonates – plus particulièrement les plus puissants d'entre eux, à savoir l'alendronate et le risédronate – réduisent efficacement les risques de fracture chez les sujets à haut risque, et ces effets bénéfiques apparaissent dès la première année de thérapie.
Déclarations sommaires
21. Chez les femmes ménopausées souffrant d'ostéoporose,
a. l'alendronate85,117,118,127,133 et le risédronate38,136,137 sont efficaces pour prévenir les fractures vertébrales et non vertébrales [niveau 1];
b. l'alendronate117 et le risédronate38 préviennent les fractures de la hanche chez les femmes ménopausées souffrant d'ostéoporose sévère [niveau 1];
c. l'alendronate84,85,86,114,117,118,119,120,122,123,125,127,128,130,131,132,133 et le risédronate38,83,136,137,138 accroissent la DMO de la colonne vertébrale et de la hanche [niveau 1];
d. l'étidronate est efficace pour prévenir les fractures vertébrales111,113 [niveau 2];
e. l'étidronate accroÎt la DMO de la colonne vertébrale et maintient celle du col fémoral111,113 [niveau 1].
22. Chez les femmes en début de ménopause qui risquent de développer une ostéoporose, l'alendronate123,125, le risédronate135 et l'étidronate103,107,108,109 sont efficaces pour maintenir ou augmenter la DMO de la colonne vertébrale et du col fémoral [niveau 1].
23. Chez les hommes souffrant d'ostéoporose,
a. l'alendronate est efficace pour prévenir les fractures vertébrales142 [niveau 1];
b. l'alendronate142 [niveau 1] et l'étidronate164 [niveau 3] accroissent la DMO de la colonne vertébrale; l'alendronate142 augmente la DMO du col fémoral [niveau 1] et l'étidronate164 la maintient [niveau 3].
24. Dans le cas de l'ostéoporose induite par les glucocorticoïdes,
a. chez les femmes ménopausées, l'alendronate, l'étidronate et le risédronate sont efficaces pour prévenir les fractures vertébrales144,156,158,161,162,163 [niveau 1];
b. chez les hommes, le risédronate143 est efficace pour prévenir les fractures vertébrales[niveau 2];
c. l'alendronate158,159, l'étidronate144,156 et le risédronate161,163 accroissent la DMO de la colonne vertébrale et maintiennent ou augmentent celle de la hanche [niveau 1].
Recommandations
11. Les bisphosphonates sont une thérapie préventive de première intention pour les femmes ménopausées ayant une densité minérale osseuse basse, qu'il s'agisse de l'alendronate [catégorie A], de l'étidronate [catégorie A] ou du risédronate [homologué au Canada à des fins de prévention, mais les données qui s'y rapportent n'ont été publiées jusqu'ici que sous forme d'abrégé].
12. Les bisphosphonates sont une thérapie de première intention pour les femmes ménopausées souffrant d'ostéoporose, plus particulièrement celles qui présentent des fractures vertébrales préexistantes : alendronate [catégorie A], risédronate [catégorie A] et étidronate [catégorie B].
13. Les bisphosphonates sont la thérapie de première intention pour prévenir l'ostéoporose induite par les glucocorticoïdes : alendronate [catégorie A], risédronate [catégorie A] et étidronate [catégorie A].
14. Les bisphosphonates sont la thérapie de première intention pour le traitement de l'ostéoporose induite par les glucocorticoïdes chez les sujets exigeant une thérapie prolongée aux glucocorticoïdes : alendronate [catégorie A], risédronate [catégorie A] et étidronate [catégorie B].
15. Les bisphosphonates sont la thérapie de première intention pour les hommes ayant une masse osseuse basse ou une ostéoporose : alendronate [catégorie A] et étidronate [catégorie B].
16. Chez les femmes préménopausées ayant une ostéopénie ou une ostéoporose, l'utilisation des bisphosphonates n'a pas été évaluée et les bisphosphonates ne sont pas encore recommandés en l'absence de cause secondaire documentée de l'ostéoporose. Il demeure toutefois que, dans certaines circonstances, on peut songer à les employer. Faute de données probantes sur l'innocuité de ces agents médicamenteux en période de grossesse, l'utilisation d'un moyen de contraception serait prudente et le traitement devrait être cessé en cas de grossesse [catégorie D].
Calcitonine
La calcitonine est une hormone peptidique présente à l'état naturel. On ne comprend pas encore bien le rôle physiologique précis qu'elle joue dans la santé des adultes, mais à des doses pharmacologiques cette substance inhibe l'activité ostéoclastique et sa fonction est donc celle d'un antirésorptif.
Étant un polypeptide, la calcitonine ne peut s'administrer par voie orale. On l'a initialement administrée par injection165,166. Cette voie d'administration s'accompagnait d'effets secondaires multiples, ce qui devait en restreindre l'utilisation dans le traitement à long terme de l'ostéoporose. On a constaté qu'une insufflation nasale permettant à la calcitonine de passer par la muqueuse nasale causait moins d'effets secondaires167.
Puisque la calcitonine de poisson a un effet plus puissant sur les humains que la calcitonine humaine, la calcitonine de saumon recombinée est devenue la forme chimique type de cet agent médicamenteux165,166,167.
Traitement à la calcitonine des femmes ménopausées souffrant d'ostéoporose : Nous avons recensé 25 comptes rendus d'ERC portant sur l'administration de calcitonine à des femmes ménopausées souffrant d'ostéoporose116,119,168,169,170,171,172,173,174,175,176,177,178,179,180,181,182,183,184,185,186,187,188,189,190,191. Dans la plupart, on utilisait de la calcitonine de saumon en insufflation. Les résultats fondés sur des paramètres substitutifs, tels les marqueurs biochimiques du remodelage osseux ou l'ostéodensitométrie, étaient généralement convergents entre les diverses études : le traitement à la calcitonine donnait lieu à une diminution modeste mais reproductible de la résorption osseuse (de 5 % à 20 % plus que dans le groupe placebo) et à une augmentation de la DMO (de 1 % à 8 % plus que dans le groupe placebo) sur une période de 1 à 5 ans.
Une seule étude, «Prevent Recurrence of Osteoporotic Fractures» (étude PROOF)168, présentait le degré voulu de puissance et était conçue pour détecter un changement dans les taux de fractures. Dans cette étude, l'administration quotidienne de 200 UI de calcitonine de saumon intranasale causait une diminution significative de 33 % à 36 % du nombre de fractures vertébrales. Il s'agissait là d'un ERC prospectif, mais les résultats ont néanmoins été caractérisés comme des données probantes de niveau 2, car on s'interrogeait sur l'absence d'effet dose-réponse (il n'y avait aucune diminution significative du nombre de fractures à une dose quotidienne de 400 UI) et sur le taux élevé d'abandon des sujets. L'étude n'avait pas la puissance nécessaire pour déceler une réduction des fractures non vertébrales.
Plusieurs autres études172,174,175 ont produit des données qui indiquent une réduction des fractures vertébrales dans les groupes traités avec la calcitonine, mais le type d'étude ou l'analyse de leurs données ne satisfaisait pas aux critères d'un ERC de niveau 1.
La calcitonine dans la prévention de l'ostéoporose postménopausique : Pour la plupart, les études portant sur l'administration de calcitonine n'indiquent pas suffisamment comment la population étudiée se rangerait dans les catégories actuelles de diagnostic. Puisque l'on n'a répertorié aucune étude qui traitait définitivement de la prévention de l'ostéoporose chez les femmes ménopausées, la calcitonine ne peut être recommandée pour un tel cadre de prévention.
Administration de calcitonine aux femmes préménopausées : Dans un ERC191, on s'est attaché à l'efficacité de l'administration de calcitonine à des femmes préménopausées. On n'a constaté aucun avantage, mais la dose de calcitonine de saumon intranasale était inférieure à la dose reconnue efficace. Donc, bien que manquant de données probantes, nous pouvons considérer la calcitonine comme une option thérapeutique chez les femmes préménopausées en raison de son profil d'innocuité et de l'absence d'alternative thérapeutique dans ce groupe.
Calcitonine et ostéoporose induite par les glucocorticoïdes : On a étudié la calcitonine tant pour la prévention que pour le traitement de l'ostéoporose induite par les glucocorticoïdes. Quatre études ont porté sur la calcitonine de saumon administrée par voie intranasale et trois autres, sur la calcitonine injectable192,193,194,195,196,197,198. Dans les études de prévention, la calcitonine réduisait la perte osseuse causée par les glucocorticoïdes, mais ne produisait pas de gain net de DMO193,194,198. Chez des sujets atteints d'ostéoporose ou traités aux glucocorticoïdes sur une longue période, la calcitonine produisait en revanche un gain net de DMO192,195,196,197. Nous ne disposons cependant d'aucune donnée sur les fractures pour l'un et l'autre de ces groupes. On peut donc dire que, si la calcitonine injectable ou intranasale peut servir à la prévention ou au traitement de l'ostéoporose induite par les glucocorticoïdes, ce n'est pas une pharmacothérapie de premier choix, car il existe, pour d'autres agents médicamenteux, des données au sujet des effets sur les fractures.
Calcitonine et douleur associée à la fracture vertébrale : Quatre ERC199,200,201,202 ont démontré que la calcitonine atténue la douleur que causent les fractures vertébrales aiguës. On a examiné sous cet angle la calcitonine de saumon injectable (deux études) et intranasale (deux études). On a évalué les sujets 3 à 14 jours après une fracture. Au cours des trois premiers jours de traitement, la douleur était significativement plus faible dans le groupe calcitonine que dans le groupe placebo. Au bout de 7 à 10 jours, les sujets présentaient une amélioration marquée; l'effet bénéfique était maintenu pendant 28 jours (ce qui correspond à la durée de l'étude la plus longue). La dose quotidienne de calcitonine injectable était de 100 UI, alors qu'elle était de 200 UI pour la calcitonine intranasale. La comparaison simultanée des deux préparations a montré l'équivalence de ces doses203. Il n'y a pas de données appréciables sur l'effet analgésique pour d'autres types de fractures ou pour les fractures vertébrales chroniques.
Effets secondaires : La seule contre-indication absolue pour l'administration de calcitonine de saumon intranasale ou injectable est une hypersensibilité connue à la calcitonine ou au véhicule pharmaceutique165,166,167. Dans des essais sur les animaux, la calcitonine a causé une insuffisance pondérale à la naissance, lorsqu'administrée en période de grossesse; elle a aussi réduit la production de lait maternel lorsque donnée en période de lactation165,166,167. En l'absence de données chez l'humain, on devrait éviter la calcitonine en période de grossesse ou d'allaitement.
On a signalé des réactions anaphylactiques et d'autres réactions allergiques graves, mais elles sont rares pour les deux formulations. On peut faire un test cutané avec une dose diluée de calcitonine avant d'administrer la pleine dose, bien que ce ne soit pas là la pratique clinique normale pour la préparation intranasale165,166,167.
Jusqu'à 30 % des gens qui prennent, sur une période de cinq ans, de la calcitonine de saumon intranasale présenteront des irritations nasales. On pourra également observer de légers saignements de nez (moins de 15 %), des symptômes variés de dérèglement des voies nasales (moins de 15 %) et des ulcérations nasales (moins de 5 %). La plupart de ces effets secondaires sont légers ou modérés et n'entraÎnent pas l'arrêt du traitement. Les effets secondaires sérieux sont rares (moins de 1 %)167.
Les effets indésirables sont plus fréquents avec la calcitonine injectable qu'avec la calcitonine intranasale. Les plus courants sont les nausées ou les vomissements (moins de 40 %), les rougeurs au visage (moins de 35 %) et les éruptions cutanées au site d'injection (moins de 10 %)165,166. Bien qu'exemptes de gravité, ces manifestations peuvent mener à une interruption de traitement. Les effets sérieux sont rares (moins de 1 %)165,166.
Les anticorps contre la calcitonine se développent chez les gens traités avec l'une ou l'autre des préparations, et ceci en fonction des doses utilisées. Toutefois, ils ne semblent pas agir sur l'efficacité de la calcitonine ni s'accompagner d'effets secondaires, et on n'a donc pas à les surveiller165,166,167,168.
Déclarations sommaires
25. La calcitonine intranasale est efficace pour prévenir les fractures vertébrales chez les femmes ménopausées souffrant d'ostéoporose sévère168 [niveau 2]. Elle maintient ou accroÎt minimalement la DMO de la hanche et de la colonne vertébrale116,119,168,170,171,172,173,174,175,176,177,178,179,180,181,182,183,184,185,186,187,188,189,190,191 [niveau 1]. L'efficacité de la calcitonine intranasale dans la prévention des fractures non vertébrales n'a pas été démontrée168 [niveau 2].
26. Chez les sujets ayant récemment entrepris une thérapie aux glucocorticoïdes, la calcitonine ralentit la perte osseuse à tous les sites et la prévient à certains193,194,198 [niveau 2].
27. Chez les sujets souffrant d'une ostéoporose induite par les glucocorticoïdes, la calcitonine maintient ou accroÎt la DMO192,195,196,197 [niveau 2].
28. La calcitonine est efficace pour réduire la douleur causée par les fractures vertébrales aiguës199,200,201,202 [niveau 1].
Recommandations
17. La calcitonine intranasale est une thérapie de seconde intention pour les femmes ménopausées souffrant d'ostéoporose [catégorie B].
18. En raison de son profil d'innocuité, on peut songer à administrer la calcitonine intranasale à des femmes préménopausées qui ne sont pas enceintes et qui souffrent d'ostéoporose [catégorie D].
19. On peut songer à administrer la calcitonine intranasale aux hommes souffrant d'ostéoporose [catégorie D].
20. L'administration de calcitonine par voie intranasale ou parentérale est une thérapie analgésique de première intention pour les douleurs reliées aux fractures vertébrales aiguës [catégorie A].
Hormonothérapie substitutive pour les femmes ménopausées
Pour la SOC, les termes «hormonothérapie substitutive» (HTS) et «hormonothérapie ovarienne» (HTO) sont synonymes. Les femmes ménopausées ne sont pas en déficit hormonal, puisque les faibles concentrations d'œstrogènes et de progestérone représentent un phénomène normal. Le mot «substitutif» ne convient donc pas. Toutefois, afin de se conformer à l'usage international, la SOC désigne par le sigle «HTS» la thérapie combinée aux œstrogènes et à la progestine-progestérone.
L'HTS (ou les œstrogènes seuls ou la progestérone seule) sert le plus souvent à soulager les bouffées de chaleur et les sueurs nocturnes (symptômes vasomoteurs) que provoque la diminution des concentrations d'œstrogènes et de progestérone. Toutes les doses, toutes les préparations et toutes les diverses formes d'HTS sont efficaces pour réduire les symptômes vasomoteurs204.
La phase de perte osseuse accélérée s'amorce au moment où les menstruations deviennent irrégulières durant la périménopause205 et elle se poursuit pendant quatre à cinq ans, et parfois jusqu'à dix ans après la ménopause206. Chez les femmes ménopausées, l'HTS est efficace pour mettre fin à cette perte osseuse et pour accroÎtre la DMO à tous les sites anatomiques mesurés.
L'âge moyen de la ménopause (on définit celle-ci comme l'absence de menstruations pendant un an) est d'environ 51 ans. Les femmes qui connaissent une ménopause précoce (avant l'âge de 40 ans) ou relativement précoce (avant l'âge de 45 ans) courent plus de risques de souffrir d'ostéoporose207. Voilà pourquoi l'HTS est importante chez les femmes qui sont ménopausées avant l'âge de 45 ans.
L'HTS a été utilisée pendant plus de 60 ans pour traiter l'ostéoporose et encore récemment, il s'agissait du principal traitement. Néanmoins, les données probantes issues d'essais cliniques portant sur son efficacité ont été sous optimales. Les résultats des premiers essais cliniques ayant porté sur les bisphosphonates ont été rendus publics dans les années 1990, mais jusqu'à la dernière décennie, les modèles d'essais cliniques thérapeutiques ont été des études de cohortes, de cas témoins ou des études épidémiologiques chez des femmes ménopausées ayant demandé l'HTS ou à qui leur médecin avait prescrit cette thérapie. Les femmes qui ont déclaré recevoir l'HTS étaient aussi celles qui étaient fidèles au traitement. Nous savons aujourd'hui que des essais cliniques avec de tels modèles prêtent à des biais de cohorte saine et de conformité au traitement qui peuvent faire paraÎtre une thérapie plus efficace qu'elle ne l'est en réalité208.
Jusqu'à tout récemment, un seul essai clinique modeste, d'une durée d'un an, portant sur les œstrogènes administrés par voie transdermique avec un échantillonnage aléatoire, à double insu et contrôlé par placebo209, a démontré une prévention des fractures vertébrales, et ce, bien que l'étude ait eu un certain nombre de problèmes d'ordre méthodologique. Il n'y a pas eu d'ERC conçu pour démontrer la prévention des fractures de la hanche. Aux États-Unis, on a interrompu de façon prématurée un important essai clinique prospectif avec échantillonnage aléatoire, à double insu et contrôlé par placebo (Women's Health Initiative)210 en raison d'un rapport risques–avantages défavorable de la thérapie combinée œstrogènes–progestérone (Prémarin et Provera); on a constaté une augmentation significative du risque relatif de maladie coronarienne (rapport de probabilités [RP] 1,29; IC nominal de 95 % 1,02 à 1,63), de cancer du sein envahissant (RP 1,26; IC 1,00 à 1,59), d'accident vasculaire cérébral (RP 1,41; IC 1,07 à 1,85) et de thromboembolie veineuse (RP 2,11; IC 1,58 à 2,82) même si les risques absolus individuels étaient faibles bien que significativement plus élevés dans le groupe traité. Du côté des aspects positifs, on a finalement pu démontrer que l'administration continue d'œstrogènes et de progestérone causait une diminution significative du risque de fracture à tous les sites, y compris à la hanche (RP 0,66; IC 0,45 à 0,98), et de cancer colorectal (RP 0,63; IC 0,43 à 0,92). On a interrompu seulement le volet «thérapie combinée aux œstrogènes-progestérone» de l'étude. Le volet «œstrogénothérapie seule»210 se poursuit et livrera un complément d'information.
Au nombre des risques importants de la thérapie combinée aux œstrogènes et progestine-progestérone, on compte la thromboembolie veineuse210,211 et les cancers du sein et de l'endomètre212,213,214,215,216. Chez les utilisatrices actuelles, ce traitement accroÎt les risques de cancer du sein s'il est suivi pendant plus de cinq ans après la ménopause. Il y a une augmentation des risques de saignements vaginaux irréguliers et de cancer de l'endomètre si l'on prend des œstrogènes sans progestine-progestérone ou avec des doses insuffisantes de progestine-progestérone. Le risque absolu d'embolie pulmonaire, par 10 000 personnes-années, attribuable à l'HTS est accru de 8 événements et celui de toutes les thromboembolies veineuses, est accru de 18 événements210.
Déclarations sommaires
29. Chez les femmes ménopausées souffrant d'ostéoporose, l'HTS est efficace pour prévenir les fractures vertébrales cliniques209,210 et les fractures non vertébrales, y compris celles de la hanche210 [niveau 1].
30. Chez les femmes ménopausées, l'HTS est efficace pour accroÎtre la DMO à tous les sites88,217,218,219,220 [niveau 1].
31. Chez les utilisatrices actuelles, l'HTS prise pendant plus de cinq ans après la ménopause accroÎt les risques de cancer du sein envahissant, de maladie coronarienne et d'accident vasculaire cérébral de 26 %, 29 % et 41 % respectivement210 [niveau 1].
32. L'utilisation d'œstrogènes sans progestine-progestérone accroÎt les risques de saignements vaginaux irréguliers et de cancer de l'endomètre210,212,213,214,215,216 [niveau 1].
33. L'HTS accroÎt le risque de thromboembolie veineuse, le nombre d'événements sur une période de 5 ans passant de 16 par 10 000 personnes-années dans le groupe placebo à 34 par 10 000 personnes-années dans le groupe HTS210 [niveau 1].
34. L'HTS est efficace dans le traitement des symptômes vasomoteurs204 [niveau 1].
Recommandations
21. L'HTS est une thérapie préventive de première intention pour les femmes ménopausées ayant une densité minérale osseuse basse. Cependant, si on utilise l'HTS uniquement pour la prévention de l'ostéoporose postménopausique, ses risques peuvent l'emporter sur ses avantages [catégorie A].
22. L'HTS est une thérapie préventive de première intention pour les femmes ménopausées avant l'âge de 45 ans [catégorie D].
23. L'HTS est une thérapie de seconde intention pour les femmes ménopausées souffrant d'ostéoporose [catégorie B]. Si l'HTS est prise longtemps pour le seul traitement de l'ostéoporose postménopausique, les risques appréciables de maladie cardiovasculaire, d'accident vasculaire cérébral et de cancer du sein envahissant peuvent entraÎner un rapport risques–avantages défavorable.
Modulateurs sélectifs des récepteurs œstrogéniques
Les modulateurs sélectifs des récepteurs œstrogéniques (MSRE) sont des agents non hormonaux qui se lient aux récepteurs œstrogéniques avec une affinité équivalente à celle de l'œstradiol, mais qui ont des effets agonistes des œstrogènes dans certains tissus et des effets antagonistes dans d'autres. La structure de tout ligand est un facteur important qui détermine les changements de conformation se produisant dans le récepteur œstrogénique lorsque le ligand s'y lie. Chaque ligand semble donner une forme finale différente au récepteur œstrogénique. Cette forme détermine les interactions avec des cofacteurs protéiques et des éléments de réponse de l'ADN qui se traduisent à la fin par des effets tissulaires spécifiques, agonistes ou antagonistes221.
Le raloxifène est le seul MSRE homologué pour la prévention et le traitement de l'ostéoporose. Il s'administre sous forme d'un comprimé unique (60 mg par jour) indépendamment des repas, des suppléments de calcium et de vitamine D ou de l'heure du jour. Il a des effets agonistes des œstrogènes sur les os et le métabolisme des lipides et des effets antagonistes des œstrogènes sur le sein et l'utérus.
Effets sur le squelette : Un important ERC (étude MORE ou «Multiple Outcomes of Raloxifene Evaluation»)35 a évalué l'efficacité antifracturaire de cet agent chez les femmes ménopausées depuis plusieurs années et souffrant d'ostéoporose (score T inférieur à -2,5 à la colonne lombaire ou au col fémoral). Le raloxifène a réduit de façon significative l'incidence de nouvelles fractures vertébrales chez les femmes avec (réduction de 30 %) ou sans (réduction de 50 %) fracture vertébrale préexistante. De plus, le raloxifène a réduit de façon significative l'incidence de deux nouvelles fractures vertébrales ou plus dans les deux groupes. Cependant, le risque de fracture non vertébrale n'a pas été réduit de façon significative. Par rapport au groupe placebo, le raloxifène a produit une augmentation significative de la DMO à la colonne lombaire et au col fémoral, ainsi qu'une diminution significative des marqueurs du remodelage osseux.
Dans une analyse rétrospective222 portant sur un faible nombre d'événements fracturaires, on a constaté, par rapport au groupe placebo, que le raloxifène abaissait de 68 % les risques de nouvelles fractures vertébrales cliniques sur un an. Mentionnons en outre que les données relatives à la quatrième année de l'étude MORE semblent indiquer que le raloxifène a une efficacité soutenue contre les fractures vertébrales223.
Effets extrasquelettiques : Par rapport au groupe placebo, le raloxifène administré pendant deux ans a entraÎné une diminution significative du cholestérol total et du cholestérol des lipoprotéines de densité faible)224. Il n'y avait pas de différences significatives pour le cholestérol des lipoprotéines de densité élevée (HDL), ni pour les concentrations de triglycérides. Les résultats sur quatre ans de l'étude MORE révélaient des effets semblables sur les concentrations lipidiques225. La prise de raloxifène pendant quatre ans n'a eu aucune influence significative sur le risque global de maladie cardiovasculaire dans l'ensemble de la population, mais elle a entraÎné une diminution significative de ce risque chez les femmes à haut risque et chez celles qui présentaient une maladie cardiovasculaire établie. À la différence de l'HTS226, l'administration de raloxifène ne semblait pas causer une augmentation précoce du risque d'événements cardiovasculaires, bien que les événements aient été trop peu nombreux dans la première année pour que l'on puisse tirer des conclusions définitives. Il est nécessaire d'obtenir des essais cliniques prospectifs, sur échantillon aléatoire, d'une puissance suffisante, et avec des événements cardiovasculaires comme issues prédéterminées, avant de pouvoir recommander l'utilisation du raloxifène pour la prévention des maladies cardiovasculaires.
Le raloxifène a diminué d'une manière significative (84 %) l'incidence du cancer du sein envahissant à récepteurs œstrogéniques positifs après quatre ans chez les femmes ménopausées atteintes d'ostéoporose qui étaient à faible risque de cancer du sein227. Un complément d'observation confirme cet effet protecteur. Il indique qu'il faudrait traiter 93 femmes au raloxifène pendant 4 ans pour prévenir un cas de cancer du sein envahissant227. Là encore, on a besoin d'un ERC prospectif chez les femmes à haut risque de cancer du sein avant que le raloxifène ne soit recommandé pour la prévention du cancer du sein. On n'a pas étudié ce composé chez les femmes ayant déjà eu un cancer du sein, ni chez les femmes qui sont encore menstruées.
Effets secondaires : Le raloxifène semble généralement sûr et bien toléré par l'organisme. Les patientes qui ont pris du raloxifène ont rapporté une augmentation des bouffées de chaleur et des crampes aux jambes par rapport au groupe placebo228,229, mais ces symptômes étaient habituellement légers à modérés et ne suffisaient pas à faire interrompre le traitement. On n'a constaté aucun lien entre les crampes aux jambes et les risques de thromboembolie veineuse. Contrairement aux œstrogènes et au tamoxifène, le raloxifène n'accroissait ni les saignements vaginaux ni le cancer de l'endomètre par rapport au groupe placebo228,229,230,231.
La thromboembolie veineuse représente un effet secondaire sérieux du raloxifène, bien que les cas déclarés soient peu fréquents (1,44 et 3,32 événements pour 1000 personnes-années respectivement dans le groupe placebo et le groupe raloxifène à une dose de 60 mg par jour)227. L'ordre de grandeur du risque relatif est semblable à celui observé tant avec l'HTS210,211 qu'avec le tamoxifène232. Le raloxifène est contre-indiqué dans le cas des sujets ayant déjà subi une thromboembolie veineuse. Il serait prudent de cesser cette médication trois jours avant toute immobilisation prolongée.
Le raloxifène constitue une thérapie de première intention pour la prévention et le traitement de l'ostéoporose chez les femmes ménopausées. En cas de confirmation d'effets extrasquelettiques favorables dans de nouvelles études, le raloxifène serait de nature à accroÎtre les avantages globaux d'une intervention thérapeutique auprès des femmes ménopausées qui ont un faible risque de fracture à court terme.
Déclarations sommaires
35. Le raloxifène est efficace pour prévenir les fractures vertébrales chez les femmes ménopausées souffrant d'ostéoporose35,223 [niveau 1]. Il accroÎt la DMO de la colonne vertébrale et du col fémoral35,223 [niveau 1]. On n'a pas encore démontré son efficacité dans la prévention des fractures non vertébrales35 [niveau 2].
36. Chez les femmes ménopausées souffrant d'ostéoporose, le raloxifène diminue l'incidence du cancer du sein envahissant à récepteurs œstrogéniques positifs227,228 [niveau 1]. Toutefois, le raloxifène n'est pas encore recommandé pour la prévention ou le traitement du cancer du sein.
37. Le raloxifène n'accroÎt pas les risques d'hyperplasie endométriale ou de cancer de l'endomètre228,230,231 [niveau 1].
38. Le raloxifène accroÎt les risques de thromboembolie veineuse de 1,44 à 3,32 événements pour 1000 personnes-années227 [niveau 1].
39. Le raloxifène n'a pas d'effet bénéfique sur les symptômes vasomoteurs et il est susceptible d'en accroÎtre l'incidence228,229 [niveau 1].
Recommandations
24. Le raloxifène est une thérapie de première intention pour la prévention de la perte osseuse subséquente chez les femmes ménopausées ayant une DMO basse [catégorie A].
25. Le raloxifène est une thérapie de première intention pour les femmes ménopausées souffrant d'ostéoporose [catégorie A].
Thérapies parallèles ou complémentaires
Les thérapies parallèles sont celles qui ne sont pas encore intégrées à la médecine classique233. À l'heure actuelle, les traitements à la vitamine K et à l'ipriflavone sont les seules thérapies parallèles pour lesquelles il y a suffisamment de données sur leurs effets sur la DMO et les fractures pour justifier leur inclusion dans des lignes directrices clinique sur l'ostéoporose.
Ipriflavone — un phytoœstrogène de synthèse : Les phytoœstrogènes sont des agents chimiques d'origine végétale qui ressemblent aux œstrogènes et qui présentent des effets agonistes et antagonistes des œstrogènes. Trois principaux groupes de phytoœstrogènes sont présents à l'état naturel, à savoir les isoflavones (que l'on trouve principalement dans la fève de soya et d'autres légumineuses), les lignanes (que l'on trouve principalement dans les graines de lin, les fruits et les légumes) et les coumestans (que l'on trouve dans les germes de soya et les plantes fourragères). Les études épidémiologiques semblent indiquer que les populations qui consomment des quantités importantes de phytoœstrogènes (comme les Asiatiques habitant en Asie) ont des taux de fractures de la hanche plus faibles que les Nord-américains234. Toutefois, il y a très peu de données probantes directes au sujet de l'effet protecteur des phytoœstrogènes naturels chez l'humain.
On dispose de beaucoup plus de données sur un phytoœstrogène de synthèse, l'ipriflavone235,236,237,238,239,240,241,242,243,244,245,246,247,248,249. Il est difficile de comparer les essais cliniques sur l'ipriflavone en raison des différences dans les techniques utilisées pour mesurer la DMO et les sites mesurés. L'interprétation des résultats de ces études se trouve également limitée par le fait que les ERC sur l'ipriflavone n'ont pas prévu dans tous les cas un apport suffisant de calcium et de vitamine D dans le groupe traité ou le groupe placebo. De plus, il manque de données sur les effets à long terme de l'ipriflavone sur d'autres tissus sensibles à l'action œstrogénique (sein et utérus); la plus grande étude menée à ce jour247 semble indiquer que la consommation d'ipriflavone est liée à une lymphopénie appréciable chez 29 des 237 femmes traitées. Les effets sur les fractures n'ont été évalués que dans une seule étude247. On n'a démontré aucune différence dans la survenue de fractures vertébrales chez les femmes qui prenaient de l'ipriflavone par rapport au groupe placebo, mais seulement un petit nombre de femmes ont subi des fractures vertébrales pendant la période de suivi de 36 mois. D'autres études plus importantes s'avèrent nécessaires avant de pouvoir établir si l'ipriflavone protège contre les fractures vertébrales.
Déclarations sommaires
40. Il est difficile de comparer les essais cliniques sur l'ipriflavone comme moyen de prévention de la perte osseuse et des fractures chez les femmes ménopausées en raison des différences dans les techniques utilisées pour mesurer la DMO et dans les sites mesurés235,236,237,238,239,240,241,242,243,244,245,246,247,248,249.
41. L'ipriflavone (200 mg, 3 fois/jour) est efficace pour maintenir la DMO de la colonne vertébrale chez les femmes ménopausées235,239 [niveau 1].
42. L'ipriflavone n'est pas efficace pour prévenir les fractures chez les femmes ménopausées souffrant d'ostéoporose247 [niveau 2].
43. L'ipriflavone n'a pas été étudiée chez les hommes ou chez les femmes préménopausées.
Recommandations
26. L'ipriflavone peut être considérée comme une thérapie préventive de seconde intention chez les femmes ménopausées [catégorie B].
27. L'ipriflavone n'est pas recommandée pour le traitement des femmes ménopausées souffrant d'ostéoporose [catégorie B].
28. Puisque les données probantes sur l'innocuité à long terme de l'ipriflavone sont peu concluantes, les sujets qui en prennent doivent être surveillés de près [catégorie B].
29. L'ipriflavone n'est pas recommandée chez les hommes ou chez les femmes préménopausées [catégorie D].
Vitamine K : On trouve à l'état naturel deux types de vitamine K, à savoir la vitamine K1 dans des plantes comme la laitue et la vitamine K2 dans la viande, le fromage et les produits de fermentation. La vitamine K joue un rôle important dans la fonction des protéines osseuses. Les concentrations circulantes de vitamine K sont plus faibles chez les sujets ayant subi une fracture de la hanche par rapport aux témoins; les études d'observation semblent indiquer qu'un apport alimentaire élevé en vitamine K est associé à un risque de fracture de la hanche plus faible250,251. Ces constatations ont conduit à des ERC qui se sont intéressés aux effets d'un traitement à la vitamine K sur la DMO ou les fractures252,253,254,255,256. Ces études sont limitées par le fait que les ERC consacrés à la vitamine K (habituellement ménatétrénone 45 mg par jour) n'ont pas évalué l'apport de calcium ou de vitamine D dans le groupe traité ou le groupe placebo.
Déclarations sommaires
44. La vitamine K n'est pas efficace pour prévenir la perte osseuse liée à l'insuffisance ovarienne d'origine médicamenteuse252 [niveau 2].
45. La vitamine K peut être efficace pour ralentir la perte osseuse chez les femmes ménopausées souffrant d'ostéoporose, mais on n'a pas démontré sa supériorité sur le calcium et la vitamine D255,256 [niveau 1].
46. La vitamine K peut être efficace pour traiter les femmes ménopausées souffrant d'ostéoporose sévère, mais on n'a pas démontré sa supériorité sur le calcium et la vitamine D254 [niveau 2].
47. La vitamine K n'a pas été étudiée chez les hommes ou chez les femmes préménopausées.
Recommandations
30. La vitamine K n'est pas recommandée actuellement pour la prévention de l'ostéoporose postménopausique [catégorie B].
31. La vitamine K n'est pas recommandée actuellement pour le traitement des femmes ménopausées souffrant d'ostéoporose [catégorie B].
32. L'utilisation de la vitamine K n'est pas recommandée chez les hommes ou chez les femmes préménopausées [catégorie D].
Fluor
Le fluorure de sodium est un stimulateur puissant de la formation osseuse. On l'a étudié initialement comme traitement de l'ostéoporose en 1964257. Cette substance a gagné en popularité dans les années 1970 et 1980258. Ce fût le premier agent pour lequel on a rapporté qu'il était capable d'accroÎtre la DMO axiale chez les patients souffrant d'ostéoporose259, et ce, principalement dans des études non contrôlées. En 1989, un rapport consensuel260 a fait part d'un optimisme prudent quant à l'efficacité de la thérapie au fluor, tout en reconnaissant la grande fréquence des effets secondaires, notamment dans le cas de certaines préparations.
Les années 1990 ont été marquées par l'apparition des ERC dans la recherche sur l'ostéoporose, et par l'utilisation de mesures morphométriques précises des fractures vertébrales. Toutefois, les composés de fluor n'ont pas été évalués de façon adéquate en utilisant des normes modernes de collecte de données probantes. Presque toutes les études en question ont été modestes et d'une puissance restreinte. Il faut ajouter que le profil clinique du traitement au fluor varie considérablement selon les composés et les préparations pharmacologiques pour ce qui est de la biodisponibilité et des effets secondaires. Ainsi, les études qui existent ne sont pas comparables pour la plupart.
Le fluor dans le traitement des femmes ménopausées : Cinq ERC ont évalué la thérapie au fluor dans la prévention des fractures vertébrales chez les femmes ménopausées261,262,263,264,265. Ces essais cliniques étaient d'une durée variable (de deux à quatre ans), ils faisaient appel à des préparations pharmacologiques de fluor différentes (fluorure de sodium ordinaire ou à délitage entérique, monofluorophosphate de sodium et fluor à libération lente), et à des doses différentes de fluor, de sorte qu'ils n'étaient pas comparables. Cependant, aucune étude n'a démontré une diminution significative des fractures vertébrales malgré des augmentations constantes et significatives de la DMO vertébrale pouvant atteindre jusqu'à 6 à 8 % par année. Dans une petite étude à répartition aléatoire263 portant sur une thérapie au fluor à libération lente, on a prétendu démontrer une diminution des fractures vertébrales en exprimant les données en taux de fractures par groupes sans faire voir une réduction significative du nombre de femmes présentant de nouvelles fractures vertébrales. Avec la thérapie au fluor, même un accroissement majeur de la DMO ne saurait être considéré comme un indicateur substitutif de la prévention des fractures. On n'a pas démontré que la thérapie au fluorure de sodium était utile pour prévenir les fractures dans l'ostéoporose postménopausique, et il n'y a eu aucune étude chez les femmes préménopausées.
Thérapie au fluor pour les hommes : Dans un petit ERC266, on a réparti de façon égale, entre un groupe traité et un groupe témoin, 60 hommes âgés en moyenne de 52 ans et présentant un score T moyen de -2,74 à la colonne lombaire. Le groupe traité a reçu 114 mg de monofluorophosphate de sodium par jour (15 mg de fluor à l'état ionique) selon une alternance de trois mois de traitement et d'un mois sans traitement. Au bout de 36 mois, le nombre de patients ayant des fractures vertébrales avait diminué de 75% (12 patients avaient subi des fractures vertébrales dans le groupe témoin contre 4 dans le groupe traité). Dans le groupe traité, dix patients ont présenté des effets indésirables. Cet ERC unique démontrant l'existence d'un effet sur les fractures chez les hommes contraste avec les résultats négatifs obtenus chez les femmes. Il est improbable que les effets d'un traitement au fluor soient différents chez les hommes et les femmes, et il n'y a pas de données probantes directes à ce sujet. Aussi doit-on en conclure que l'on n'a pas encore su prouver l'efficacité antifracturaire de la thérapie au fluor dans l'ostéoporose.
Fluor et ostéoporose induite par les glucocorticoïdes : Dans quatre ERC ayant porté sur un traitement au fluor dans l'ostéoporose induite par les glucocorticoïdes267,268,269,270, on a démontré des augmentations de deux à dix fois de la DMO vertébrale au bout d'un ou deux ans de traitement au fluor. Ces études étaient toutefois trop modestes pour montrer un effet antifracturaire significatif.
Toxicité : Les effets toxiques du fluor sont proportionnels aux doses et la prévalence des effets indésirables varie selon les préparations pharmacologiques. Dans cinq des études déjà mentionnées261,262,264,265,271, les patients présentaient une toxicité gastro-intestinale (gastralgies et nausées) et squelettique (douleurs aux membres inférieurs et fractures d'insuffisance) à des taux significativement différents par rapport au groupe témoin. La toxicité était particulièrement liée au fluorure de sodium ordinaire et au monofluorophosphate de sodium264,265. L'une et l'autre de ces préparations peuvent produire des effets secondaires gastro-intestinaux et squelettiques. Il y avait beaucoup moins d'effets secondaires gastro-intestinaux dans le cas des préparations à délitage entérique262 et encore moins avec la préparation au fluor à libération lente263.
Déclarations sommaires
48. Il n'a pas été démontré que les préparations au fluor réduisaient les fractures vertébrales ou non vertébrales chez les femmes ménopausées souffrant d'ostéoporose261,262,264,265, malgré des augmentations constantes et durables de la DMO vertébrale261,262,263,264,265. Les préparations de fluor maintiennent ou accroissent de façon marginale la DMO du col fémoral262,263,264,265 [niveau 1].
Recommandations
33. Le fluor n'est pas recommandé pour le traitement des femmes ménopausées souffrant d'ostéoporose [catégorie A].
34. Le fluor n'est pas recommandé chez les femmes préménopausées ou chez les hommes [catégorie D].
Parathormone
On a décrit l'utilisation clinique de la parathormone (PTH) dans le traitement de l'ostéoporose en 1980272, mais son développement commercial a été retardé jusqu'à l'avènement de l'ostéodensitométrie centrale par DXA, laquelle permettait une évaluation rapide de son efficacité sur l'accroissement de la masse osseuse. Son fragment synthétique N-terminal, hPTH(1-34), a été utilisé presque exclusivement dans les études publiées, ainsi que dans les essais cliniques pharmaceutiques de la tériparatide rhPTH(1-34). Au moment où nous écrivons ces lignes, on s'attendait à ce que la tériparatide reçoive l'approbation des organismes américains de réglementation et que l'homologation s'en fasse sous peu dans d'autres pays, dont le Canada. Une autre parathormone contenant la séquence d'aminoacides rhPTH(1-84) fait actuellement l'objet d'une évaluation de phase III.
PTH et traitement de l'ostéoporose postménopausique : L'ERC charnière de la tériparatide273 a évalué son efficacité pour réduire le nombre de fractures vertébrales et non vertébrales chez 1637 femmes ménopausées présentant au moins une fracture vertébrale à l'entrée dans l'étude. Cet essai a pris fin de façon prématuré après une période médiane de 21 mois en raison de la survenue d'ostéosarcomes dans une étude de toxicologie à long terme chez des rats auxquels on avait administré de fortes doses de tériparatide de leur petite enfance à leur sénescence (voir plus loin).
La diminution du nombre de fractures dépendait du type de fractures analysées. Par rapport au groupe placebo, le risque relatif de nouvelles fractures vertébrales était d'environ 0,35. Chez les femmes présentant des fractures vertébrales variant de modérées à sévères, le risque d'en subir de nouvelles (déformations radiographiques) était réduit jusqu'à 90 %. Dans le cas des fractures non vertébrales, le risque relatif s'établissait à 0,47 sans qu'on sache laquelle de deux doses (20 ou 40 μg par jour en injection sous-cutanée) donnait les meilleurs résultats273. Par rapport au groupe placebo, la tériparatide causait une augmentation proportionnelle aux doses de la DMO à la colonne lombaire (10 à 14 %) aussi bien qu'au col fémoral ou à la hanche totale(3 à 4 %)273. Bien que d'autres petits ERC ayant porté sur l'hPTH(1-34) n'aient pas eu la puissance voulue pour une évaluer l'efficacité antifracturaire, on a observé des augmentations constantes et semblables de la DMO à la colonne vertébrale et à la hanche sur des périodes de traitement de un à trois ans274,275,276.
PTH et ostéoporose masculine : Il y a peu de données permettant d'évaluer les effets de la PTH dans l'ostéoporose masculine. Dans une petite étude non contrôlée sur une cohorte de 8 hommes souffrant d'ostéoporose sévère, Slovik et coll.277 ont signalé, au bout de 12 mois de thérapie à la PTH(1-34), un gain important de DMO à la colonne lombaire (mesuré par tomodensitométrie quantitative), mais sans augmentation significative de la DMO à l'avant-bras. Dans un petit ERC d'une durée de 18 mois278, la PTH(1-34) a causé une augmentation de 13,5 % de la DMO de la colonne lombaire chez 10 hommes présentant une ostéoporose sévère par rapport à un groupe témoin de 13 hommes recevant seulement des injections de placebo avec du calcium et de la vitamine D. On a mesuré la DMO par la technique DXA. On a également présenté des données provisoires sur l'utilisation de la tériparatide dans un ERC réalisé sur 437 hommes dans le cadre d'essais cliniques réglementaires279. On a observé sur une période de 12 mois une augmentation de la DMO mesurée par la technique DXA qui était proportionnelle aux doses de PTH et qui variait entre 6 % et 9 % pour la colonne lombaire et entre 2 % et 3 % pour le col fémoral. Les changements étaient non significatifs dans le groupe placebo. Dans l'essai sur la tériparatide, le gain de DMO à la colonne lombaire rappelait les changements observés dans un essai plus important consacré aux femmes ménopausées273. Ces études ont duré 18 mois ou moins et n'avaient pas la puissance voulue pour évaluer l'efficacité antifracturaire. Il demeure que les gains comparables de DMO chez les hommes et les femmes ménopausées laissent prévoir une efficacité antifracturaire similaire.
PTH et ostéoporose induite par les glucocorticoïdes : Jusqu'à présent, la seule étude sur la PTH et l'ostéoporose secondaire est un ERC d'une durée de 12 mois ayant porté sur 51 femmes ménopausées souffrant d'ostéoporose induite par les glucocorticoïdes280. Toutes ces femmes recevaient une œstrogénothérapie chronique et avaient reçu des doses cliniquement significatives de prednisone sur une période moyenne de 12 à 15 ans; près du tiers présentaient des fractures vertébrales au début de l'essai. Par rapport au groupe témoin sous œstrogénothérapie, le traitement à la PTH(1-34) a entraÎné une augmentation significative (11,1 %) de la DMO à la colonne lombaire, ainsi qu'une augmentation moyenne non significative de 2,9 % de la DMO au col fémoral. Un suivi de la cohorte pendant 12 autres mois, alors qu'elle continuait l'œstrogénothérapie, a permis d'observer un léger accroissement additionnel de la DMO dans le groupe traité antérieurement avec la PTH(1-34)281. Malgré le risque apparent élevé de nouvelle fracture dans cette cohorte, on a observé très peu de fractures vertébrales ou de fractures cliniques. De toute manière, l'essai était trop modeste pour évaluer l'efficacité antifracturaire de la PTH.
Les effets secondaires en cours de traitement avec la PTH ont été relativement rares. La douleur et l'induration aux sites d'injection étaient vraisemblablement dues au véhicule ayant servi à reconstituer le peptide274,275, et elles n'ont pas été relevées dans le cas de la tériparatide273. Pendant les essais cliniques sur la tériparatide, on a constaté, de façon peu fréquente, des nausées, des maux de tête, des étourdissements et des crampes aux jambes comme effets secondaires proportionnels aux doses273. On ne s'étonnera pas que les propriétés pharmacologiques de la PTH aient provoqué des épisodes occasionnels d'hypercalcémie ou d'hypercalciurie en cours d'essais, ce qui a été corrigé par l'arrêt des suppléments de calcium ou une légère réduction de la posologie273. À ce jour, les données des études de toxicologie sur la tériparatide faisant état de la survenue tardive d'ostéosarcomes chez les rats ayant reçu de fortes doses de rhPTH(1-34) de la petite enfance à la sénescence n'ont pas été relevées dans les études correspondantes chez les humains. À l'heure actuelle, on s'accorde à dire qu'une exposition restreinte (sur un à deux ans) à un traitement de PTH chez les gens plus âgés souffrant d'ostéoporose ne fait pas courir à cette population le risque de développer des ostéosarcomes ou autres néoplasies.
Déclarations sommaires
49. L'hPTH(1-34) est efficace pour prévenir les fractures vertébrales et non vertébrales chez les femmes ménopausées souffrant d'ostéoporose sévère273. L'hPTH (1-34) accroÎt la DMO à tous les sites du squelette à l'exception du radius273 [niveau 1].
50. Chez les hommes souffrant d'ostéoporose sévère, l'hPTH(1-34) accroÎt la DMO à la colonne vertébrale277,278,279 [niveau 2].
51. Chez les femmes ménopausées souffrant d'ostéoporose induite par les glucocorticoïdes, l'hPTH(1-34) accroÎt la DMO à la colonne vertébrale280 [niveau 2].
Recommandations
35. L'hPTH(1-34) n'est pas encore un agent homologué au Canada, mais on s'attend à ce que son administration devienne une thérapie de première intention pour les femmes ménopausées souffrant d'ostéoporose sévère [catégorie A].
36. On s'attend également à ce que l'administration d'hPTH(1-34) devienne une thérapie recommandée pour les hommes et pour les sujets souffrant d'ostéoporose sévère en raison d'une thérapie prolongée aux glucocorticoïdes [catégorie D].
Interventions non pharmacologiques
Nutrition
Le comité sectoriel sur la nutrition avait pour mandat d'établir si le calcium, la vitamine D et certains autres facteurs nutritionnels étaient susceptibles d'être utilisés pour la prévention et le traitement de l'ostéoporose (Figure 3). On s'est interrogé sur l'effet de l'apport d'éléments nutritifs et d'autres composés alimentaires sur l'acquisition ultérieure du pic de masse osseuse, ainsi que sur la prévention de la perte osseuse et des fractures. Un premier bilan documentaire a permis de relever 16 058 abrégés. De ce nombre, on a examiné 996 études. La base de données probantes ainsi constituée comprenait 56 études sur la vitamine D, le calcium ou les deux, et 26 études sur d'autres éléments nutritifs et composés reliés à l'alimentation.
Fig. 3 : Traitement optimal de l'ostéoporose chez les femmes ménopausées. Note : *Principalement, la fracture vertébrale. On a démontré que seuls l'alendronate et le risédronate et, récemment, l'HTS en administration continue, diminuent les risques de fracture de la hanche.
Les recommandations relatives aux apports d'éléments nutritifs ont été évaluées sous l'angle de leurs effets sur la santé osseuse. Les autres rôles des éléments nutritifs n'ont pas été examinés. Si un élément nutritif essentiel n'avait pas d'effet apparent sur l'os, nous avons recommandé qu'aucun apport additionnel n'est nécessaire, sachant que l'os est un tissu complexe exigeant la présence de tous les éléments nutritifs essentiels pour sa synthèse et son maintien. Puisqu'il manque de données sur les niveaux d'apports nutritifs nécessaires à la croissance osseuse du bébé et de l'enfant, nos recommandations visent seulement les adultes, sauf avis contraire. Les recommandations sur les apports représentent des objectifs individuels en matière d'alimentation. Les valeurs proposées sont les quantités les plus basses ou les quantités utiles uniformément signalées dans les essais cliniques, et ce, en sus des quantités de base des éléments nutritifs. Ainsi, nos recommandations portent sur l'apport diététique total.
Déclarations sommaires
Calcium et vitamine D
52. Un apport adéquat en calcium et vitamine D, par la diète ou les suppléments, est essentiel à la prévention de l'ostéoporose et, pris ensemble, constituent un complément essentiel à la thérapie préventive107,108,109,123,125,230,282 [niveau 1].
53. L'apport en calcium et vitamine D ne doit pas être utilisé comme seul traitement de l'ostéoporose; toutefois, l'apport en calcium et vitamine D, par la diète ou les suppléments, constitue un complément essentiel au traitement de l'ostéoporose35,38,85,106,113,117,118,136,137,283,284,285 [niveau 1].
54. L'apport calcique recommandé en provenance de toutes les sources («toutes les sources» s'entend de la diète globale et des suppléments) est le suivant :
a. enfants prépubertaires (4 à 8 ans) : 800 mg/jour286,287,288,289 [niveau 1];
b. adolescents (9 à 18 ans) : 1300 mg/jour287,290,291,292 [niveau 1];
c. femmes préménopausées : 1000 mg/jour293,294,295 [niveau 1];
d. hommes après l'adolescence jusqu'à l'âge de 50 ans : 1000 mg/jour296,297 [niveau 3];
e. femmes ménopausées : 1500 mg/jour282,283,284,285,298,299,300,301,302,303,304,305 [niveau 1];
f. hommes de plus de 50 ans : 1500 mg/jour285,296,297 [niveau 1];
g. femmes de 18 ans et plus en période de grossesse ou de lactation : même dose que pour les adultes en dehors de la période de grossesse, à savoir 1000 mg/jour306,307,308,309 [niveau 1].
55. La vitamine D3 (cholécalciférol) doit être préférée à la vitamine D2 (ergocalciférol)310 [niveau 2].
56. Chez les Canadiens, l'exposition au soleil ne semble pas suffire à remplacer les apports alimentaires de vitamine D311 [niveau 3].
57. L'apport en vitamine D recommandé en provenance de toutes les sources («toutes les sources» s'entend de la diète globale et des suppléments) est le suivant :
a. hommes et femmes âgés de 19 à 50 ans : 400 UI (10 μg)/jour311,312,313 [niveau 4];
b. hommes et femmes de plus de 50 ans : 800 UI (20 μg)/jour282,283,284,285,314 [niveau 1].
Macroéléments nutritifs : protéines, acides gras et fibres alimentaires
58. L'augmentation de l'apport en protéines chez ceux qui ont un apport alimentaire inadéquat en protéines a un effet favorable sur le risque de fracture de la hanche chez les hommes et chez les femmes315,316 [niveau 3].
59. Il n'y a pas de données probantes de bonne qualité qui confirment ou infirment les effets favorables des acides gras essentiels ou des fibres alimentaires sur la DMO ou sur le risque de fracture.
Éléments nutritifs reliés au mode de vie : caféine et sel
60. Une consommation abondante de caféine (plus de quatre tasses de café par jour) est en corrélation significative avec la fracture de la hanche chez les hommes et chez les femmes317,318 [niveau 2].
61. Les effets du sodium sur la DMO sont ambivalents; cependant, dans les études où l'apport sodique fait l'objet d'une mesure appropriée, on constate une corrélation négative significative chez les femmes319 [niveau 3] et chez les hommes320 [niveau 5] lorsque cet apport est de plus de 2100 mg par jour (90 mmol).
Autres oligo-éléments
62. Tant chez les hommes que chez les femmes ayant une digestion normale, le surcroÎt d'apport alimentaire en magnésium n'a pas d'effet significatif sur le risque de fracture de la hanche296,321,322,323 [niveau 3].
63. Chez les hommes et chez les femmes ménopausées, le surcroÎt d'apport alimentaire en cuivre n'a aucun effet significatif sur le risque de fracture de la hanche296,324 [niveau 3].
64. Il n'y a pas d'association significative entre le risque de fracture et l'apport en zinc chez les hommes325 [niveau 3], et un surcroÎt d'apport alimentaire en zinc n'a pas d'effet significatif sur la DMO chez les femmes322 [niveau 5].
65. Il n'y a pas de données probantes de bonne qualité qui confirment ou infirment les effets favorables des apports en fer sur la DMO ou sur le risque de fracture; toutefois, chez les femmes de plus de 39 ans, un apport riche en fer (plus de 30 mg par jour) pourrait être lié à une augmentation du risque de fracture de la hanche326 [niveau 4].
66. Il y a peu d'études qui ont convenablement traité des apports alimentaires de phosphore. Dans la fourchette des valeurs normales de l'apport quotidien, et ce, sans égard aux additifs phosphatés dans les aliments transformés, il ne semble pas y avoir de rapport significatif entre l'apport en phosphore et les fractures de la hanche chez les hommes325 [niveau 3], d'une part, et la DMO chez les femmes320 [niveau 5], d'autre part.
67. Il n'y a pas de données probantes de bonne qualité qui confirment ou infirment les effets sur la DMO ou le risque de fracture des apports alimentaires en silice, bore ou strontium, ou d'un surcroÎt en manganèse.
Recommandations
37. Les apports quotidiens suivants en calcium sont recommandés:
a. enfants prépubertaires (4 à 8 ans) : 800 mg/jour [catégorie B];
b. adolescents (9 à 18 ans) : 1300 mg/jour [catégorie B];
c. femmes (19 à 50 ans) : 1000 mg/jour [catégorie A];
d. femmes de plus de 50 ans : 1500 mg/jour [catégorie A];
e. femmes en période de grossesse ou de lactation (18 ans et plus) : 1000 mg/jour [catégorie A];
f. hommes (19 à 50 ans) : 1000 mg/jour [catégorie C];
g. hommes de plus de 50 ans : 1500 mg/jour [catégorie C].
38. Les apports quotidiens suivants en vitamine D3 sont recommandés:
a. femmes (19 à 50 ans) : 400 UI (10 μg)/jour [catégorie D];
b. femmes de plus de 50 ans : 800 UI (20 μg)/jour [catégorie A];
c. femmes en période de grossesse ou de lactation (18 ans et plus) : 400 UI (10 μg)/jour [catégorie D];
d. hommes (19 à 50 ans) : 400 UI (10 μg)/jour [catégorie D];
e. hommes de plus de 50 ans : 800 UI (20 μg)/jour [catégorie A].
Nous précisons qu'il s'agit de la vitamine D3, puisque ses effets sont plus puissants que ceux de la vitamine D2; pour se conformer à nos recommandations, il faudrait donc prendre plus de vitamine D2.
39. Il est important de maintenir un apport suffisant de protéines [catégorie C].
40. On doit éviter les excès de caféine (plus de quatre tasses de café par jour) [catégorie B].
41. On doit éviter les excès de sodium alimentaire (plus de 2100 mg/jour ou de 90 mmol/jour), car cela réduit la DMO chez les hommes et les femmes d'âge adulte [catégorie C].
42. Il n'y a pas de données probantes permettant de recommander un surcroÎt de l'apport des éléments nutritifs suivants pour la prévention ou le traitement de l'ostéoporose : magnésium, cuivre, zinc, phosphore, manganèse, fer et acides gras essentiels [catégorie D].
Activité physique et prévention des chutes
L'activité physique profite à la structure et la résistance du squelette, et on connaÎt bien les effets préjudiciables de l'immobilisation. L'activité physique varie en caractère, en fréquence, en durée, en intensité et selon l'âge de son début. Son impact est différent sur les différentes parties du squelette, et ce, en fonction du modèle des forces qui s'exercent. Une autre complication est que, en influant sur l'état hormonal, surtout chez les femmes préménopausées, et peut-être à cause d'une sous-nutrition associée, l'excès d'activité peut nuire au squelette.
Les sports sont la forme la plus extrême de l'activité physique normalement entreprise, mais par nature ils ne se prêtent pas à des ERC. On les classe principalement dans deux catégories d'activité physique: il y a, d'une part, les activités aérobiques ou avec impact (jogging, sports de terrain ou de raquettes, gymnastique) et, d'autre part, les activités d'endurance ou de renforcement (haltérophilie, culturisme, natation, cyclisme et exercices sur appareils fixes). On peut donc juger de la nature des activités physiques qui auront le plus de chance d'être salutaires.
Activité physique et DMO
Enfants, avant et pendant la puberté : La question du plus grand intérêt est probablement celle de savoir si l'activité physique peut apporter un changement permanent au squelette de manière à produire des bienfaits pour le reste de la vie. Il est clair qu'on a la meilleure chance d'obtenir ce résultat à l'époque de la croissance. Chez les enfants, l'interprétation des changements de DMO est difficile, puisque la méthode habituelle de mesure de DMO (technique DXA) est sensible aux dimensions, ayant tendance à sous-estimer la densité des petits os et à surestimer celle des gros os. Il importe donc d'apparier les «cas» et les «témoins» en fonction du stade de croissance et de l'état pubertaire et de tenir compte de tout effet de l'activité physique sur la croissance, ce qui pourrait se manifester, par exemple, par un retard pubertaire.
Un ERC assez important et assez long pour donner une réponse définitive à cette question n'existe pas et n'existera sans doute jamais. Nous devons rassembler les éléments de réponse du mieux qu'on le peut à partir des données disponibles.
Deux ERC, l'un sur les garçons et l'autre sur les filles de 9 à 12 ans, ont démontré qu'un programme d'exercices d'une durée de 7 mois, comportant des sauts, produira des changements de la DMO et de certaines mesures des dimensions du squelette. Chez les filles, l'effet s'est révélé plus marqué en début de puberté que plus tôt dans leur vie327,328; cependant l'effet bénéfique ne se limite pas à l'époque de la puberté, mais peut aussi s'obtenir chez les plus jeunes329,330,331. La plupart des sports auxquels s'adonnent les enfants sont des activités avec impact comme le base-ball, le basket-ball et le soccer et se trouvent associés à une amélioration de la DMO. La gymnastique est particulièrement utile. Des activités sans impact, comme la natation ou l'entraÎnement en renforcement, ne sont guère bienfaisantes à cet égard332,333.
Jeunes adultes après la puberté : On constate les avantages d'exercices avec impact chez les jeunes adultes après la puberté334,335,336,337. On relève les meilleurs résultats chez ceux qui ont fait de l'exercice durant toute leur enfance338. La course donne des résultats variables tant chez les hommes (voir plus loin) que chez les femmes selon la nutrition et l'état hormonal. Khan et coll. ont examiné cet effet chez les jeunes femmes339.
On se rend compte aussi que l'haltérophilie produit des résultats inégaux dans le cas des jeunes adultes340,341. Les jeunes athlètes olympiques masculins en haltérophilie présentaient une DMO supérieure, bien qu'on ait par ailleurs signalé dans leur cas un éventuel recours aux stéroïdes anabolisants342,343.
Adultes plus âgés — hommes, femmes préménopausées et ménopausées : Des études cas témoins344,345,346,347,348 ont indiqué des accroissements variables de la DMO chez les hommes pratiquant des sports. Il reste que nombre de ces études ont comme sujets des adultes qui se vouent à l'activité sportive depuis l'enfance349,350,351. Dans une étude portant sur les hommes d'âge adulte qui jouaient au tennis, on a observé une DMO supérieure de 15 % à la colonne lombaire et de 11 % au fémur proximal349. En ce qui concerne la course à pied sur longue distance, on constate un effet bénéfique chez les gens qui courent de 15 à 20 milles par semaine; pour une raison quelconque, de plus grandes distances ne sont guère avantageuses et se trouvent en réalité à réduire la densité osseuse352,353,354. La plupart des études d'intervention chez les hommes sont des études cas témoins sans répartition aléatoire. On a grand besoin d'essais cliniques à répartition aléatoire, à grande échelle et sur de longues périodes.
Une méta-analyse355 de 8 ERC (d'une durée de 6 à 36 mois) auprès de femmes préménopausées (âgées de 16 à 44 ans) visait à déterminer si les exercices avec impact réduisaient la perte osseuse reliée au vieillissement par opposition aux exercices sans impact. Les exercices avec impact étaient notamment des exercices aérobiques à impact élevé, tels la course à pied et l'entraÎnement au saut. Parmi les exercices sans impact, on comptait les étirements, les entraÎnements en renforcement et l'haltérophilie. Les études se trouvaient limitées par de petites tailles d'échantillon et des taux élevés d'abandon des sujets. La perte osseuse à la colonne lombaire était réduite de 1,5 % (IC à 95 % : 0,6 % à 2,4 %) dans le groupe d'exercices avec impact et de 1,2 % (IC à 95 % : 0,7 % à 1,7 %) dans le groupe d'exercices sans impact. Dans une étude ayant porté sur de jeunes collégiennes, on a constaté que la course à pied (avec impact) et l'haltérophilie (sans impact) étaient tout autant utiles pour diminuer la perte osseuse356. Somme toute, les études dans lesquelles la fidélité à l'activité était élevée présentaient la plus grande influence sur le maintien ou l'amélioration de la DMO.
Les études portant sur les femmes ménopausées sont généralement modestes et de courte durée, mais il y a beaucoup plus d'ERC dans ce cas. Comme dans ces études on tente de changer les habitudes en matière d'activité physique, la fidélité devient un problème à résoudre, bien que, dans les conditions propres à ces études, les taux d'observance soient habituellement relativement élevés (50 % à 100 %). La plupart des chercheurs ont étudié l'influence de l'activité physique chez les gens qui participaient pleinement par opposition à ceux qui étaient moins dociles et aux témoins. Ainsi, ces études s'attachent à l'efficacité plutôt qu'à l'utilité et ne comportent pas d'analyses de l'intention de traitement.
La marche à pas rapide, la danse et les sauts semblent ralentir ou prévenir la perte osseuse chez les femmes ménopausées, bien que les résultats obtenus ne soient pas entièrement convergents300,357,358,359,360,361,362,363,364,365,366. Les activités physiques destinées à accroÎtre la force et l'endurance, ou la force des muscles spécifiques qui agissent sur les os en question (il s'agit le plus souvent d'haltérophilie ou d'exercice sur appareils fixes) donnent des résultats inégaux367,368,369,370,371,372,373,374. On ne sait au juste quels sont les avantages possibles de l'activité physique en synergie avec l'hormonothérapie substitutive, les résultats demeurant hétérogènes là aussi363,375,376.
On a consacré quelques méta-analyses à l'effet de l'activité physique sur la perte osseuse chez les femmes ménopausées. Wolff et coll.377 sont parvenus à la conclusion que l'activité physique prévenait ou renversait environ 1% de la perte osseuse annuelle, aussi bien à la colonne lombaire qu'au col fémoral. Plusieurs autres méta-analyses355,378 ont trouvé un avantage supérieur à l'activité physique pour la colonne vertébrale, et ce, plus particulièrement au regard des exercices avec impact. Certains exercices avec impact peuvent aussi agir favorablement sur la DMO de la hanche, mais l'existence d'un effet des exercices sans impact sur la DMO de la hanche reste encore à démontrer355.
Activité physique et prévention des fractures : Les études cas-témoins379,380 portant sur les sujets âgés, victimes de fractures de la hanche, montrent que ceux-ci se sont moins adonnés à l'activité physique tout au long de leur vie adulte. Dans une grande étude d'observation prospective381, on a relevé des taux de perte osseuse à la hanche plus élevés chez les gens les plus inactifs (confinés au lit ou au fauteuil roulant). Dans une étude prospective382 menée auprès de 9012 hommes sur une période de 7 ans, on a dénombré moins de fractures de fragilisation chez les hommes qui faisaient davantage d'exercices avec mise en charge. L'activité physique intense (définie comme étant plus que la marche) était liée à une diminution de l'incidence des fractures de la hanche dans le groupe le plus actif (RP 0,38; IC à 95 % : 0,16 à 0,91) dans une étude de cohorte d'une durée de 21 ans383.
Il n'y a pas d'ERC prospectifs à long terme évaluant les effets de l'activité physique sur la survenue de fractures.
Activité physique et prévention des chutes : Chez les adultes âgés de plus de 65 ans et vivant seuls, on a démontré que l'activité physique diminuait le nombre de chutes384. Il peut notamment s'agir de programmes personnalisés de renforcement musculaire progressif, d'exercices de réadaptation de l'équilibre ou de plans de marche propres à réduire, sur une période d'un an, le nombre de gens qui tombent ou qui subissent des blessures à la suite de chutes (RR 0,80; IC à 95 % : 0,66 à 0,98). Il y également eu moins de chutes chez ceux qui poursuivaient les activités physiques pendant une deuxième année385,386,387.
On a aussi démontré une réduction des chutes avec le Tai-chi388. Toutefois, lorsqu'on a redéfini les chutes pour en exclure les événements mineurs comme les trébuchements, les résultats n'étaient plus statistiquement significatifs.
Les programmes d'exercices de groupe, non personnalisés, ne semblent pas aussi utiles pour réduire le nombre de chutes, et d'autres études sont nécessaires dans ce domaine.
Autres programmes permettant de réduire les chutes : Chez les personnes âgées ayant des antécédents de chutes, on a démontré qu'un programme d'évaluation des risques de chute au foyer et de réaménagement des lieux, tel que prescrit par un(e) ergothérapeute, diminuait le risque de chute survenant à l'intérieur comme à l'extérieur du foyer (RR 0,64; IC à 95 % : 0,49 à 0,84)389. Ceux qui n'avaient pas d'antécédents de chutes ne retiraient aucun avantage d'un tel programme.
L'arrêt des psychotropes est également utile pour réduire le nombre de chutes chez les personnes âgées vivant à domicile386.
Les programmes préventifs de visites éducatives à domicile (évaluation des facteurs médicaux, fonctionnels, psychosociaux et environnementaux et les recommandations qui en découlent) ne se sont pas avérés utiles pour prévenir les chutes chez les personnes âgées habitant leur domicile390.
Les programmes polyvalents à l'intention des personnes âgées qui habitent à domicile sont utiles pour réduire le nombre de chutes (RR (données groupées) 0,79; IC à 95 % : 0,67 à 0,94) chez ceux qui ont des antécédents de chutes ou des facteurs de risque de chute384,391,392. Ajoutons que Tinetti et coll.393 ont constaté une baisse du nombre de chutes (rapport du taux d'incidence ajusté de 0,69; IC à 95 % : 0,52 à 0,90), dans le cas d'une intervention polyvalente. De telles interventions consistent notamment en un dépistage des facteurs de risque pour la santé et des facteurs de risque dans l'environnement, une évaluation de l'activité physique et des dangers au foyer et une modification ou un arrêt des psychotropes. Ces programmes ont produit des effets favorables seulement en Amérique du Nord, ce qui pourrait être dû à des différences dans les systèmes de santé et des différences dans les catégories d'interventions polyvalentes et multidisciplinaires.
Déclarations sommaires
68. Les enfants qui font de l'exercice ont habituellement des os plus résistants que ceux qui n'en font pas329,331,338,394 [niveau 3].
69. Faire de l'exercice en période de puberté peut être particulièrement efficace pour constituer un squelette plus résistant327,328 [niveau 1].
70. Les exercices avec impact entraÎnent une amélioration de la DMO autant chez les garçons que chez les filles327,328 [niveau 1].
71. Les exercices avec impact et les sports qui comportent de tels exercices sont plus efficaces à tout âge que les exercices de renforcement ou d'endurance ou les activités sans mise en charge332,333,359 [niveau 4].
72. Chez les hommes, l'activité physique est liée à des DMO plus élevées, et c'est le cas en particulier pour l'activité physique avec impact344,345,346,347,348 [niveau 4].
73. Chez les femmes préménopausées, autant les exercices avec impact que ceux sans impact préviennent la perte osseuse à la colonne lombaire, les exercices avec impact étant quelque peu plus bénéfiques355,356 [niveau 2+].
74. Chez les femmes ménopausées, les exercices avec impact peuvent réduire les taux de perte osseuse ou conduire à un certain gain de masse osseuse, du moins à court terme. La réponse aux exercices sans impact ou aux exercices en endurance est moindre et plus inégale300,357,358,359,360,364,365,367,368,371,372,373 [niveau 1].
75. Autant chez les hommes que chez les femmes, un excès d'activité physique comme la course à pied sur longue distance peut être préjudiciable352,353,354 [niveau 4].
76. Un degré supérieur d'activité physique au milieu de la vie est lié à un risque réduit de fracture de la hanche au cours de la vieillesse [consensus].
77. Les programmes d'exercices personnalisés qui prévoient un renforcement musculaire, une réadaptation de l'équilibre et de la marche, sur une période d'un an, sont utiles pour réduire le nombre de chutes384,385,386,387 [niveau 1+] et les blessures qui en découlent384 [niveau 2+]. Les programmes d'exercices de groupe ne se sont pas avérés utiles pour diminuer le nombre de chutes.
78. Les programmes polyvalents qui conjuguent les interventions sont utiles pour réduire les chutes autant chez les sujets non sélectionnés que chez ceux qui ont des antécédents de chutes ou des facteurs de risque de chute384,391,392,393 [niveau 1+].
Recommandations
43. On devrait encourager les enfants, et notamment ceux qui sont en début ou en cours de puberté, à s'adonner à des exercices ou à des sports avec impact (principalement des sports de terrain ou de salle) [catégorie B].
44. On devrait inciter et les hommes et les femmes, tout au long de leur vie, à faire de l'exercice, et particulièrement des exercices avec mise en charge où il y a impact [catégorie C pour les hommes; catégorie B pour les femmes préménopausées et ménopausées].
45. On devrait mettre à la disposition des hommes et des femmes plus âgés qui sont à risque de chute ou qui ont déjà chuté des programmes personnalisés fondés sur une évaluation individuelle et prévoyant des exercices pour améliorer la force et l'équilibre et qui, s'il y a lieu, revêtent un caractère multidisciplinaire [catégorie A].
Conclusion
Ces lignes directrices de pratique clinique visent à fournir aux omnipraticiens les meilleures données probantes que puisse actuellement leur offrir la recherche clinique, afin de les aider à prendre leurs décisions quant à la prise en charge de l'ostéoporose. Dans chaque section du présent document, nous avons suivi les étapes nécessaires à l'élaboration de recommandations dans l'optique d'une médecine basée sur les données probantes. Nous avons donc défini la question, réuni et récapitulé les données probantes et nous avons porté un jugement en fonction des preuves produites. Comme dans bien d'autres domaines médicaux, les données probantes sur l'ostéoporose contenues dans la littérature médicale s'enrichissent rapidement. Nous pensons que ces lignes directrices revêtent un caractère évolutif et qu'on devra les actualiser et y intégrer les données probantes les plus récentes.
Les décisions en matière de soins de santé devraient reposer, dans la mesure du possible, sur des données probantes, et être adaptées aux besoins des patients, afin d'assurer une utilisation appropriée des ressources, une bonne observance au traitement et l'obtention de résultats optimaux. C'est ce qui fait de la médecine à la fois un art et une science.
Footnotes
-
On trouvera à la fin de cet article les listes des membres du Comité consultatif scientifique, du Comité directeur du projet de lignes directrices et des comités sectoriels.
Organismes de parrainage
Association canadienne de gérontologie
Association canadienne d'orthopédie
Diététistes du Canada
Société canadienne d'endocrinologie et métabolisme
Société canadienne de physiologie de l'exercice
Société canadienne de rhumatologie
Cet article est une traduction du document 2002 clinical practice guidelines for the diagnosis and management of osteoporosis in Canada [CMAJ 2002; 167(10 suppl):S1-S34]. Des corrections à la version anglaise de ces lignes directrices, publiées dans les numéros des 18 février, 4 mars et 18 mars 2003 (168[4-6]) du JAMC, ont été incorporées à la traduction.
Cet article a fait l'objet d'un examen par les pairs.
Collaborateurs : Des comités sectoriels ont étudié et élaboré les lignes directrices sous la supervision des Drs Jacques P. Brown et Robert G. Josse et le Comité consultatif scientifique les a examinées et approuvées. On trouvera ci-après les membres de ce comité consultatif, du Comité directeur du projet de lignes directrices et des comités sectoriels.
Supplément du JAMC inclus avec ce numéro :
Lignes directrices de pratique clinique 2002 pour le diagnostic et le traitement de l'ostéoporose au Canada
Remerciements : Nous remercions de leurs contributions respectives les membres du personnel de la SOC, et notamment Joyce Gordon, présidente-directrice générale, Sylvia Kowal, directrice de la commercialisation, des programmes et des communications, et Cathy Loveys, coordonnatrice des activités de programme. Nous remercions également de leur travail Linda Huestis, Rick Palidwor, Mary Bowyer, Jessie McGowan et Cathy Cameron. Nous sommes enfin redevables à Diane Adams et Julie Parrot de l'aide apportée dans l'exploitation des banques de données et les tâches administratives.
Les présentes lignes directrices ont été conçues sous l'égide du Comité consultatif scientifique de la Société de l'ostéoporose du Canada. Les travaux ont été facilités par un financement des sociétés suivantes : Eli Lilly Canada Inc., Merck Frosst Canada Inc., Novartis Pharmaceuticals Canada Inc., Procter and Gamble Pharmaceuticals, Aventis Pharma Inc. et Wyeth-Ayerst Canada Inc. Aucune de ces sociétés n'a joué un rôle dans la collecte, l'analyse et l'interprétation des données, ni dans la décision de parution du présent rapport.
Intérêts concurrents : Les Drs J. Brown, Josse, Bogoch, Jolly, Kaiser, Karaplis, Kendler, Khan, Murray, Ste-Marie et Yuen ont été consultants auprès de diverses sociétés pharmaceutiques. Les Drs Josse, Bogoch, Jolly, Kendler, Leslie, Ste-Marie et Yuen ont reçu des fonds de recherche d'un certain nombre de ces sociétés. Les Drs J. Brown, Josse, Bogoch, T. Brown, Derzko, Jolly, Kaiser, Karaplis, Kendler, Khan, Kvern, Leslie, Morrish, Murray, Ste-Marie et Yuen ont obtenu des honoraires de conférences et(ou) des bourses d'études de sociétés pharmaceutiques. Les Drs Josse, Derzko, Kaiser, Karaplis, Kendler, Khan, Kvern, Leslie, Murray, Ste-Marie et Yuen ont reçu des sommes de ces mêmes sources pour certains de leurs déplacements. Les autres membres du Comité consultatif scientifique n'ont pas déclaré d'intérêts concurrents.
Correspondance : Dr Jacques P. Brown, Centre de recherche du CHUL, local S-784, 2705, boul. Laurier, Ste-Foy QC G1V 4G2; télécopieur : 418-654-2142; courriel : jacques.browncrchul.ulaval.ca
Tirés à part : Société de l'ostéoporose du Canada, 33 Laird Dr., Toronto ON M4G 3S9; télécopieur : 416-696-2673; courriel : oscosteoporosis.ca
Bibliographie
- 1.↵
- 2.↵
- 3.↵
- 4.↵
- 5.↵
- 6.↵
- 7.↵
- 8.↵
- 9.↵
- 10.↵
- 11.↵
- 12.↵
- 13.↵
- 14.↵
- 15.↵
- 16.↵
- 17.↵
- 18.↵
- 19.↵
- 20.↵
- 21.↵
- 22.↵
- 23.↵
- 24.↵
- 25.↵
- 26.↵
- 27.↵
- 28.↵
- 29.↵
- 30.↵
- 31.↵
- 32.↵
- 33.↵
- 34.↵
- 35.↵
- 36.↵
- 37.↵
- 38.↵
- 39.↵
- 40.↵
- 41.↵
- 42.↵
- 43.↵
- 44.↵
- 45.↵
- 46.↵
- 47.↵
- 48.↵
- 49.↵
- 50.↵
- 51.↵
- 52.↵
- 53.↵
- 54.↵
- 55.↵
- 56.↵
- 57.↵
- 58.↵
- 59.↵
- 60.↵
- 61.↵
- 62.↵
- 63.↵
- 64.↵
- 65.↵
- 66.↵
- 67.↵
- 68.↵
- 69.↵
- 70.↵
- 71.↵
- 72.↵
- 73.↵
- 74.↵
- 75.↵
- 76.↵
- 77.↵
- 78.↵
- 79.↵
- 80.↵
- 81.↵
- 82.↵
- 83.↵
- 84.↵
- 85.↵
- 86.↵
- 87.↵
- 88.↵
- 89.↵
- 90.↵
- 91.↵
- 92.↵
- 93.↵
- 94.↵
- 95.↵
- 96.↵
- 97.↵
- 98.↵
- 99.↵
- 100.↵
- 101.↵
- 102.↵
- 103.↵
- 104.↵
- 105.↵
- 106.↵
- 107.↵
- 108.↵
- 109.↵
- 110.↵
- 111.↵
- 112.↵
- 113.↵
- 114.↵
- 115.↵
- 116.↵
- 117.↵
- 118.↵
- 119.↵
- 120.↵
- 121.↵
- 122.↵
- 123.↵
- 124.↵
- 125.↵
- 126.↵
- 127.↵
- 128.↵
- 129.↵
- 130.↵
- 131.↵
- 132.↵
- 133.↵
- 134.↵
- 135.↵
- 136.↵
- 137.↵
- 138.↵
- 139.↵
- 140.↵
- 141.↵
- 142.↵
- 143.↵
- 144.↵
- 145.↵
- 146.↵
- 147.↵
- 148.↵
- 149.↵
- 150.↵
- 151.↵
- 152.↵
- 153.↵
- 154.↵
- 155.↵
- 156.↵
- 157.↵
- 158.↵
- 159.↵
- 160.↵
- 161.↵
- 162.↵
- 163.↵
- 164.↵
- 165.↵
- 166.↵
- 167.↵
- 168.↵
- 169.↵
- 170.↵
- 171.↵
- 172.↵
- 173.↵
- 174.↵
- 175.↵
- 176.↵
- 177.↵
- 178.↵
- 179.↵
- 180.↵
- 181.↵
- 182.↵
- 183.↵
- 184.↵
- 185.↵
- 186.↵
- 187.↵
- 188.↵
- 189.↵
- 190.↵
- 191.↵
- 192.↵
- 193.↵
- 194.↵
- 195.↵
- 196.↵
- 197.↵
- 198.↵
- 199.↵
- 200.↵
- 201.↵
- 202.↵
- 203.↵
- 204.↵
- 205.↵
- 206.↵
- 207.↵
- 208.↵
- 209.↵
- 210.↵
- 211.↵
- 212.↵
- 213.↵
- 214.↵
- 215.↵
- 216.↵
- 217.↵
- 218.↵
- 219.↵
- 220.↵
- 221.↵
- 222.↵
- 223.↵
- 224.↵
- 225.↵
- 226.↵
- 227.↵
- 228.↵
- 229.↵
- 230.↵
- 231.↵
- 232.↵
- 233.↵
- 234.↵
- 235.↵
- 236.↵
- 237.↵
- 238.↵
- 239.↵
- 240.↵
- 241.↵
- 242.↵
- 243.↵
- 244.↵
- 245.↵
- 246.↵
- 247.↵
- 248.↵
- 249.↵
- 250.↵
- 251.↵
- 252.↵
- 253.↵
- 254.↵
- 255.↵
- 256.↵
- 257.↵
- 258.↵
- 259.↵
- 260.↵
- 261.↵
- 262.↵
- 263.↵
- 264.↵
- 265.↵
- 266.↵
- 267.↵
- 268.↵
- 269.↵
- 270.↵
- 271.↵
- 272.↵
- 273.↵
- 274.↵
- 275.↵
- 276.↵
- 277.↵
- 278.↵
- 279.↵
- 280.↵
- 281.↵
- 282.↵
- 283.↵
- 284.↵
- 285.↵
- 286.↵
- 287.↵
- 288.↵
- 289.↵
- 290.↵
- 291.↵
- 292.↵
- 293.↵
- 294.↵
- 295.↵
- 296.↵
- 297.↵
- 298.↵
- 299.↵
- 300.↵
- 301.↵
- 302.↵
- 303.↵
- 304.↵
- 305.↵
- 306.↵
- 307.↵
- 308.↵
- 309.↵
- 310.↵
- 311.↵
- 312.↵
- 313.↵
- 314.↵
- 315.↵
- 316.↵
- 317.↵
- 318.↵
- 319.↵
- 320.↵
- 321.↵
- 322.↵
- 323.↵
- 324.↵
- 325.↵
- 326.↵
- 327.↵
- 328.↵
- 329.↵
- 330.↵
- 331.↵
- 332.↵
- 333.↵
- 334.↵
- 335.↵
- 336.↵
- 337.↵
- 338.↵
- 339.↵
- 340.↵
- 341.↵
- 342.↵
- 343.↵
- 344.↵
- 345.↵
- 346.↵
- 347.↵
- 348.↵
- 349.↵
- 350.↵
- 351.↵
- 352.↵
- 353.↵
- 354.↵
- 355.↵
- 356.↵
- 357.↵
- 358.↵
- 359.↵
- 360.↵
- 361.↵
- 362.↵
- 363.↵
- 364.↵
- 365.↵
- 366.↵
- 367.↵
- 368.↵
- 369.↵
- 370.↵
- 371.↵
- 372.↵
- 373.↵
- 374.↵
- 375.↵
- 376.↵
- 377.↵
- 378.↵
- 379.↵
- 380.↵
- 381.↵
- 382.↵
- 383.↵
- 384.↵
- 385.↵
- 386.↵
- 387.↵
- 388.↵
- 389.↵
- 390.↵
- 391.↵
- 392.↵
- 393.↵
- 394.↵