PRODUCTOS SANITARIOS


.
REGLAMENTO MDR (EU) 2017/745
MDR – ingles
entrada en vigor: 26 mayo 2017
fecha aplicación: 26 mayo 2021
RD 192/2023
RD – ingles
entrada en vigor: 23 marzo 2023
«legacy» s/reglamento 2023/607
IIb(implante) y III -31 dic 2027
IIa, IIb(no implant) y I (ON) -31 dic 2028
sin fin periodo distribución
.
PRODUCTOS SANITARIOS IVD


.
REGLAMENTO IVDR (EU) 2017/746
IVDR – ingles
entrada en vigor: 26 mayo 2017
fecha aplicación: 26 mayo 2022
RD IVD
entrada en vigor: 2024?
«legacy»s/modificación regl. 2024/xx
clase D – 31 Dic 2027
clase C – 31 Dic 2028
clases B y As – 31 Dic 2029
sin fin periodo distribución
.
PROXIMA FORMACIÓN

Formacion «2406 – REGLAMENTO MDR y R.DECRETO 192/2023 – a 3 años de su Fecha de Aplicacion» – 24 Mayo 2024 9h-11h
El 26 de mayo 2021 es la fecha de aplicación del Reglamento MDR y desde 23 de marzo de 2023 está en vigor el nuevo Real Decreto 192/2023. En esta formación revisaremos el estado actual del reglamento y RD, así como todas las novedades focalizando en el impacto de estos cambios en los distintos agentes económicos y usuarios.
No te pierdas esta jornada donde contaremos las novedades según el nuevo reglamento y Real Decreto 192/2023 para estos periodos transitorios y como verificar el cumplimiento.
Fecha: 24 Mayo 2024, 9h a 11h en webinar en directo y 13h en teleformación
Dirigido a cualquier persona del sector de productos sanitarios. Esperamos verte ahi … ![]()

#ExpoÓptica24 y #ExpoAudio24 12-14 Abril 2024 @Expooptica la feria de la optica y la audiologia española
ExpoÓptica, Salón Internacional de Óptica, Optometría y Audiología, es la feria profesional de referencia del sector y punto de encuentro comercial para todos sus agentes en España y Portugal. Se presentan las marcas nacionales e internacionales de prestigio, que incluyen desde los últimos avances en el mundo de la óptica, la optometría y la audiología. Al ser las monturas y lentes ópticas de la clase I ahora ya todas con MDR, las lentes de contacto y audífonos aun en periodo transitorio pero muchos ya con marcado CE con MDR.
El Salón se celebra en paralelo a OPTOM, Congreso Internacional de Optometría, Contactología y Óptica Oftálmica, organizado por el Consejo General de Colegio de Ópticos-Optometristas.![]()

Exito de #EXPODENTAL2024 del 14 a 26 marzo 2022 Madrid – @ExpoDental_ by @FENIN_es
La feria de referencia a nivel internacional en España del sector dental español y europeo junto con la IDS de Colonia. Cada dos años, reúne en Madrid a empresas, asociaciones, centros de formación y universidades para mostrar a todos los profesionales de la industria las últimas novedades tecnológicas y tendencias, en un entorno cómodo, accesible e innovador tanto para visitantes como para expositores.
#EXPODENTAL2024 del 14 a 26 marzo 2022 Madrid – @ExpoDental_ by @FENIN_es
La feria de referencia a nivel internacional en España del sector dental español y europeo junto con la IDS de Colonia. Cada dos años, reúne en Madrid a empresas, asociaciones, centros de formación y universidades para mostrar a todos los profesionales de la industria las últimas novedades tecnológicas y tendencias, en un entorno cómodo, accesible e innovador tanto para visitantes como para expositores.

Team-NB publica el position paper «recommendations on the classification of devices intended to detect the presence or the exposure to SARS-CoV-2» cambio clase D a clase C
La Asociación Europea de Organismos Notificados de Productos Sanitarios TEAM-NB publica este nuevo position paper en el que indica que está de acuerdo en que la reclasificación de la clase D a una clase de riesgo inferior para el SARS-CoV-2 no pandémico es apropiada al haber declarado la OMS en fecha 5 desmayo de 2023 que el SARS-COV-2 (COVID 19) ya no era un PHEIC (public health emergency of international concern) y pasaba a fase endémica.
Teniendo en cuenta el riesgo potencial restante para las poblaciones vulnerables (en el peor de los casos) y los limitados datos disponibles para la fase pospandémica, se recomendaría una reclasificación a la clase C: esto garantizaría la aplicación de unos requisitos más estrictos en materia de PMS y evaluación del rendimiento/pruebas clínicas y una mejor protección de la seguridad de los pacientes.
También podría considerarse una nueva reclasificación a la clase B una vez que se disponga de más datos sobre la fase pospandémica, especialmente en lo que respecta al síndrome Covid persistente.
Descargue el documento del TEAM-NB aqui:![]()

Feria @CosmobeautyBCN 17 a 19 febrero 2024 para el sector de estética con productos de Anexo XVI MDR
La feria COSMOBEAUTY presenta las ultimas novedades del sector de la estética, entre los que hay diversos productos (laser depilación, IPL, radiofrecuencias, lentes contacto cosméticas, implantes mamarios, rellenos intradermicos, …) que están regulados como productos sanitarios por el reglamento MDR a partir de 22 de junio de 2023 y cuyo periodo transitorio para los legacy esta en cuenta atras. Incluye el Congreso Internacional de Estética y Spa (CIES), que se lleva a cabo durante los 3 días de evento, y que no incluye ninguna ponencia sobre el tema (la técnica del avestruz ….).![]()
nos vemos en CosmoBeauty …
2023 – Resumen Productos Sanitarios – Medical Devices Recap
Termina un año lleno de novedades y sorpresas y queremos desde aqui hacer un resumen del mismo:
– ENE – 37 ONs MDR y 8 ONs IVDR https://www.tecno-med.es/nuevo-on-mdr-0494/
– 16 FEB – Aprobada la extensión de periodos transitorios https://www.tecno-med.es/propuesta-modifi…dr-ivdr-aprobada/
– 20 MAR – Publicado Reglamento 2023/607 de modificación de plazos transitorios de MDR e IVDR https://www.tecno-med.es/reglamento-2023_…icacion-mdr-ivdr/
– 22 MAR – Publicado Real Decreto 192/2023 por el que se regulan los productos sanitarios entrando en vigor 23 marzo 2023 https://www.tecno-med.es/rd-ps-192_2023/
– 27 MAR – IMDRF International Medical Devices Regulators Forum en Bruselas https://www.tecno-med.es/imdrf-europe2023-final/
– 24 MAY – 1er Congreso SEDE Sociedad Española de Desinfección y Esterilización https://www.tecno-med.es/sede-mayo2023-completo-2/
– 26 MAY – 1er cumple aplicación IVDR y 2º cumple aplicación MDR https://www.tecno-med.es/2304-2-2/
– 20 JUN – Reglamento 2023/1194 que extiende los plazos de fin de periodos transitorios para productos Anexo XVI https://www.tecno-med.es/reglamento-exten…plazos-anexo-xvi/
– 22 JUN – Entrada en aplicación el reglamento MDR y RD 192/2023 a los productos de la lista de anexo XVI
– 18 JUL – MedtechEurope ( FENIN ) publica un modelo de «Manufacturer’s Declaration» a emitir por el fabricante https://www.tecno-med.es/manufacturer-declaration-medtech/
– 25 SET – IMDRF Berlin https://www.tecno-med.es/imdrf-europe2023berlin-2/
– 13-16 NOV – MEDICA https://www.tecno-med.es/medica2023-dia1/ https://www.tecno-med.es/medica2023-dia2/ https://www.tecno-med.es/medica2023-dia3/ https://www.tecno-med.es/medica2023-dia4/
– 22 NOV – Premios Tecnologia Sanitaria 2023 y Homenaje a Margarita Alfonsel https://www.tecno-med.es/homenaje-margarita-alfonsel/
– 30 NOV – Reunión EPSCO con tema de plazos, EUDAMED y en especial IVDR sobre la mesa https://www.tecno-med.es/epsco-30nov2023-2-2/
– 9 DIC – Aprobada la AIA Artificial Intelligence Act en el trilogo https://www.tecno-med.es/aprobada-la-aia-…as-enhorabuena-2/
– 16 DIC – Encuesta Comisión sobre estado MDR / IVDR https://www.tecno-med.es/com-survey-2023-12-2-2/ hasta 15 enero 2024
– 21 DIC – Estado proceso designación ONs https://www.tecno-med.es/estado-on-202312/
Como veis estamos totalmente enfrascados en la transición y en la cuenta atrás de 26 mayo 2024 donde sabremos que pasa con muchos de los legacy … y en mayo 2025 es cuando tenemos el fin para los clase D de IVDR …
Interesante el informe de MEDTECH sobre el sector en números
OS DESEAMOS FANTASTICO 2024 !!!
Team-NB publica el position paper «Medical Device Lifetime»
La Asociación Europea de Organismos Notificados de Productos Sanitarios TEAM-NB publica este nuevo position paper en la que nos da criterios para el establecimiento de la vida útil de productos en los que su análisis es difícil comeos software, los implantes, …
Felices Navidades !!! os deseamos desde @tecno_med

MEDICA @MEDICAtradefair 16 Nov 2023, resumen dia 4, ultimo día
16 nov 2023
Ya se termina el cuarto y último día de MEDICA,
– ayer nos fuimos todos puntuales (18h) con el anuncio de huelga de trenes pensando habría caos circulatorio … y no
– Ambiente de despedida en Aldstad (Café Madrid, …)
– vino caliente y bratwurst en Burgplatz mientras miramos el patinaje sobre hielo
read more…

MEDICA @MEDICAtradefair 15 Nov 2023, resumen dia 3
15 nov 2023
Ya se termina el tercer dia de MEDICA,
– Hoy tenemos un conclave regulatorio español Maria Alaez y Cristina Batlle dos grandes expertos en FENIN, cualquier duda aprovechad …
– se mantiene el alto nivel de visitantes, muchas reuniones y actividad en stands (seguimos yendo a saludarles y hemos de pasar varias veces para tener un hueco… )
– Ayer mucha concurrencia en la calle del Café Madrid … costó hoy llegar …
– hoy van las tarjetas de crédito en los restaurantes … (Thanks God)
– MEDICA Tech (IT, LAB, …) Forum : hoy con ciberseguridad, LDT, …
– Reencuentro con muchas caras conocidas, hoy internacionales (Elem, Monir, Ludger, Ronald, Carlos, Susana, Antonio, …)
– anunciada huelga de trenes … (nos ha fastidiado la visita a Colonia … )
– no llueve por la mañana … a ver si aguanta a la salida
mañana mas read more…

Feliz dia del trabajador – 1 de Mayo – PRCN y TR de los agentes económicos productos sanitarios españoles
Felicidades a todos los trabajadores del sector, dándolo todo para este cambio de las directivas a los reglamentos.
Animo que no hay mal ni paso de directivas a reglamentos que dure 100 años ….
ven a nuestros eventos read more…

Estos son los plazos de la propuesta de ampliación del periodo transitorio del IVDR aprobada
25 Abril 2024. El Parlamento Europeo ha respaldado actualizaciones clave de la ley sobre productos sanitarios que ayudarán a prevenir la escasez y facilitarán la transición hacia una mayor transparencia y acceso a la información. La MDCG esta elaborando varias guías y FAQ para estos nuevos plazos.
La modificación de los periodos transitorios para IVDR depende de la clase de riesgo:
– los productos con certificado IVDD tendrán un período de transición hasta diciembre de 2027
– los productos con alto riesgo para la salud pública e individual, como las pruebas de VIH o hepatitis (clase D), tendrán un período de transición hasta diciembre de 2027
– los productos con alto riesgo individual o moderado para la salud pública, como las pruebas de cáncer (clase C), tendrán un período de transición hasta diciembre de 2028;
– los productos de menor riesgo (clase B), como las pruebas de embarazo y los productos estériles (clase A), tienen un período de transición hasta diciembre de 2029.
- Antes de 26 de mayo de 2025 el fabricante ha de tener implantado un sistema de calidad.
- Deben tener una solicitud formal con un ON antes de:
- 26 mayo 2025 ps clase D
- 26 mayo 2026 ps clase C
- 26 mayo 2027 ps clase B y Aesteril
- Deben tener un contrato firmado con un ON antes de:
- 26 septiembre 2025 ps clase D
- 26 septiembre 2026 ps clase C
- 26 septiembre 2027 ps clase B y Aesteril
Los fabricantes también están obligados a notificarlo previamente si prevén una interrupción en el suministro de determinados productos sanitarios o productos sanitarios para diagnóstico in vitro. Deben facilitar esta información con 6 meses de antelación a las autoridades competentes, así como a los distribuidores y los prestadores de asistencia sanitaria. Esto les permitirá disponer de tiempo suficiente para tomar medidas que garanticen la atención a los pacientes.
Próximos pasos: El Consejo adoptará ahora formalmente el Reglamento modificativo. Entrará en vigor el día de su publicación en el Diario Oficial de la Unión Europea.

Symposium THAIS 11-12 junio 2024 Taulí Health Artificial Intelligence by @ParcTauli
Organizado por la Unidad Mixta del grupo de Nefrología Clínica, Intervencionista y Computacional del Instituto de Investigación e Innovación del Parc Taulí (I3PT) y la Escuela de Ingeniería de la Universidad Autónoma de Barcelona (UAB), es dar una amplia cobertura al campo de la Inteligencia Artificial en Salud desde una perspectiva orientada a los profesionales del entorno sanitario involucrados en esta área. Más información en la página web: https://www.tauli.cat/hospital/thais/

15 mayo 17h Presentación del Cuaderno de Buena Practica «Incorporación de la Tecnología Médica Innovadora» by Consejo Colegios Medicos Cataluña con la colaboración de @tecno_med
El Cuaderno de la Buena Praxis sobre la incorporación de tecnología médica innovadora del Consejo de Colegios de Médicos de Cataluña (CCMC) es un documento esencial para todos aquellos profesionales de la salud comprometidos con la excelencia y la mejora continua de la atención sanitaria. Es una iniciativa del Grupo de Trabajo de Buena Praxi del Grupo Interdisciplinar de Profesionales Vinculados con la Salud (GIPS).
Esta publicación es una valiosa herramienta que aborda la tipología de tecnologías médicas y el uso y los conocimientos que se derivan y representa una contribución significativa al campo de la biomedicina y de las ciencias que pivotan en torno a la medicina y al paciente.
Presentación dia 15 mayo 17h – inscripción previa obligagtoria
LUGAR:Sala de Actos del CoMB Passeig de la Bonanova, 47 Barcelona
![]()
Programa: read more…

Hoy 26 de Abril celebramos el Dia Mundial de la Propiedad Intelectual e Industrial #WorldIPDay @EU_IPO @WIPO @OEPM_es
El 26 de Abril celebramos el Día Mundial de la Propiedad Intelectual e Industrial. Es una celebración mundial que reconoce la importancia de la protección de estas para asegurar la innovación.
El sector de la Tecnología Médico-Sanitaria se suma a esta fiesta como sector puntero en innovación y desarrollo.
Feliz dia de S. Jordi – 23 de Abril os mandamos una rosa virtual y un libro de productos sanitarios …
 Descarga tu libro:
Descarga tu libro:
– MDR
– FAQ PERIODO TRANSITORIO MDR
– IVDR
– RD 192/2023
– RD IVD (borrador)
– RD publicidad (borrador)
– Guia marcado CE MDSW
– «Incorporación de la Tecnología Médica Innovadora»

@RAPSorg «RAPS 2024 Euro Convergence» 6-8 Mayo 2024 Berlin
Como cada año no te pierdas este evento
https://www.raps.org/europe-2024/home
Algunas fotos de la pasada edición read more…
@AEFI_es de 8 a 9 mayo 2024 en Madrid – participa @tecno_med en Taller 6 (9 mayo 12h) «MARCADO CE MDSW con IA»
Como cada año tenemos una cita en el 42 SYMPOSIUM AEFI https://aefi2024.com/ este año el 8 y 9 de Mayo de 2024 en Madrid. Participamos en este magnifico encuentro de profesionales con el taller: «Marcado CE de aplicaciones informáticas médicas incluyendo Inteligencia Artificial» C.Murphy y X.Canals

Las nuevas aplicaciones IA, tanto MDR como IVDR, van a tener un efecto multiplicador de la capacidad asistencial de los profesionales sanitarios permitiendo abordar la asignatura pendiente de prevención y seguimiento de pacientes. Revisaremos en este taller como se obtiene el marcado CE de estas aplicaciones IA
No te pierdas este evento, esperamos poder saludarte allí.
Os iremos informando …

@RAPSorg «RAPS 2024 Euro Convergence» 6-8 Mayo 2024 Berlin
Como cada año no te pierdas este evento
https://www.raps.org/europe-2024/home
Algunas fotos de la pasada edición
Fantásticas las jornadas de RAPS https://www.raps.org/europe-2023/home , para ponernos al día con los grandes expertos europeos. En esta imagen la interesante mesa sobre el paciente con la participación de todos los actores incluida la EMA con el Dr Juan Garcia Burgos.
Nos reunimos allí el grupo de LNG Spain

Hoy, 7 Abril, celebramos el Dia Mundial de la Salud #DíaMundialSalud #WorldHealthDay #WHO75 @SEEIC_Spain @SEIB_twit @SEISeSalud @AEIHorg @CEDifmbe @AAMI_connect @WHO_Europe @OMS_Spain @fenin_es @AEMPSgob @AEFI_es @tecno_med
El 7 de Abril celebramos el Día Mundial de la Salud – World Health Day, este año con el lema de la OMS «Mi salud, mi derecho»
Es una celebración mundial que reconoce la importante contribución de la sanidad en el bienestar de la población mundial.
El sector de la Tecnología Médico-Sanitaria se suma a esta fiesta y reivindica el acceso a la innovación y el suministro ininterrumpido de productos sanitarios.

Formacion «2407 – REGLAMENTO IVDR y R.DECRETO IVD – a 2 años de su Fecha de Aplicacion» – 24 Mayo 2024 12h-14h
El 26 de mayo 2022 es la fecha de aplicación del Reglamento IVDR y aún no tenemos nuevo Real Decreto IVD. En esta formación revisaremos el estado actual del reglamento y RD, así como todas las novedades focalizando en el impacto de estos cambios en los distintos agentes económicos y usuarios.
No te pierdas esta jornada donde contaremos las novedades según el nuevo reglamento y Real Decreto IVD (borrador) para estos periodos transitorios y como verificar el cumplimiento.
Fecha: 24 Mayo 2024, 12h a 14h en webinar en directo y 13h en teleformación
Dirigido a cualquier persona del sector de productos sanitarios. Esperamos verte ahi … ![]()

Formacion «2406 – REGLAMENTO MDR y R.DECRETO 192/2023 – a 3 años de su Fecha de Aplicacion» – 24 Mayo 2024 9h-11h
El 26 de mayo 2021 es la fecha de aplicación del Reglamento MDR y desde 23 de marzo de 2023 está en vigor el nuevo Real Decreto 192/2023. En esta formación revisaremos el estado actual del reglamento y RD, así como todas las novedades focalizando en el impacto de estos cambios en los distintos agentes económicos y usuarios.
No te pierdas esta jornada donde contaremos las novedades según el nuevo reglamento y Real Decreto 192/2023 para estos periodos transitorios y como verificar el cumplimiento.
Fecha: 24 Mayo 2024, 9h a 11h en webinar en directo y 13h en teleformación
Dirigido a cualquier persona del sector de productos sanitarios. Esperamos verte ahi … ![]()

Formación «2405 – IMPORTADORES Y DISTRIBUIDORES DE PROD.SANIT. según REQUISITOS MDR / IVDR y RD» – 18 Abr 2024 9h-14h
Ahora que nos acercamos al 26 de mayo de 2024 se vuelven mas relevantes los reglamentos MDR/IVDR y nuevo Real Decreto 192/2023 (RD IVD en borrador) que incrementan los requisitos a los importadores y distribuidores involucrados en el suministro, instalación, formación y mantenimiento de productos sanitarios. Ahora estamos en un periodo transitorio en el que importadores y distribuidores deben revisar el cumplimiento por parte del fabricante de los productos para su introducción en el mercado y liberación por el importador y comercialización por los distribuidores.
En esta formación, revisaremos las obligaciones de los importadores y distribuidores así como el impacto de los requisitos reglamentarios en toda la cadena de suministro. Tenemos la posibilidad de realizar mas actividades antes consideradas exclusivas de fabricante como reembalado y traducción de IFU según art.16 pero con requisito de sistema de calidad ISO 13485 certificado, también el registro del UDI-DI, el nuevo Registro de Comercialización de la AEMPS, …
No te pierdas esta jornada donde contaremos las novedades relativas a estas actividades según los nuevos reglamentos para estos periodos transitorios y como verificar el cumplimiento.
Fecha: 18 Abril 2024, 9h a 14h en webinar en directo y 25h en teleformación
Esperamos verte ahi … ![]()

Formación «2405 – IMPORTADORES Y DISTRIBUIDORES DE PROD.SANIT. según REQUISITOS MDR / IVDR y RD» – 18 Abr 2024 9h-14h
Los reglamentos MDR/IVDR y nuevo Real Decreto 192/2023 (RD IVD en borrador) refuerzan los requisitos a los importadores y distribuidores involucrados en el suministro, instalación, formación y mantenimiento de productos sanitarios. En esta formación, revisaremos las obligaciones de los importadores y distribuidores así como el impacto de los requisitos reglamentarios en toda la cadena de suministro. Tenemos la posibilidad de realizar mas actividades antes consideradas exclusivas de fabricante como reembalado y traducción de IFU según art.16 pero con requisito de sistema de calidad ISO 13485 certificado, también el registro del UDI-DI, el nuevo Registro de Comercialización de la AEMPS, …
No te pierdas esta jornada donde contaremos las novedades relativas a estas actividades según los nuevos reglamentos
Fecha: 18 Abril 2024, 9h a 14h en webinar en directo y 25h en teleformación
Esperamos verte ahi … ![]()

Formación «2404 – ISO 13485 y REQUISITOS de CALIDAD según MDR / IVDR y MDSAP» – 14 Mar 2024 9h-14h
Los reglamentos MDR e IVDR incluyen como requisito en su articulo 10 de un sistema de gestión de la calidad, siendo la norma armonizada con ambos reglamentos la EN ISO 13485:2016+AC:2018+A11:2021. En esta formación, focalizaremos en las obligaciones reglamentarias específicas incluyendo además de Europa las áreas reglamentarias de MDSAP y su impacto en los procesos, procedimientos y auditorÍas.
No te pierdas esta jornada donde contaremos las novedades sobre calidad en productos sanitarios
Fecha: 14 Marzo 2024, 9h a 14h en webinar en directo y 25h en teleformación
Esperamos verte ahi … ![]()
Intentamos resumir los cambios para productos sanitarios …

Formación «2405 – IMPORTADORES Y DISTRIBUIDORES DE PROD.SANIT. según REQUISITOS MDR / IVDR y RD» – 18 Abr 2024 9h-14h
Los reglamentos MDR/IVDR han reforzado los requisitos a los importadores y distribuidores involucrados en el suministro, instalación, formación y mantenimiento de productos sanitarios. En esta formación, revisaremos las obligaciones de los importadores y distribuidores así como el impacto de los requisitos reglamentarios en toda la cadena de suministro.
No te pierdas esta jornada donde contaremos las novedades relativas a estas actividades según los nuevos reglamentos
Fecha: 18 Abril 2024, 9h a 14h en webinar en directo y 25h en teleformación
Esperamos verte ahi … ![]()

Formación «2402 – COMERCIALIZACIÓN PRODUCTOS SANITARIOS USA – FDA» – 8 Feb 2024 9h-14h
El principal destino de exportación europeo de productos sanitarios es USA. Por lo que revisaremos como a partir de la documentación técnica y sistema de calidad para el Marcado CE podemos adaptarla para obtener la autorización para la comercialización en USA presentando un 510K y el cumplimiento de la 21 CFR 820 Quality System Regulations.
Con cambios muy relevantes en este ultimo año que van desde guías nuevas de evaluación de productos via 510k, guías de ensayos preclinicos y clínicos, guías QSUB, guías esterilización, guías software, …
No te pierdas esta jornada donde contaremos las novedades y como obtener el clearance de FDA y comercializar tus productos sanitarios en USA.
Fecha: 8 Febrero 2024, 9h a 14h en webinar en directo y 25h en teleformación
Esperamos verte ahi … ![]()
Intentamos resumir los cambios para productos sanitarios …

Formación AI MDSW ahora online «2401T – SOFTWARE MÉDICO e INTELIGENCIA ARTIFICIAL» con las novedades normativas y de guías
Este diciembre se aprobó el texto de la AIA Artificial Intelligence Act que incluye al software médico con IA como crítico y también diversas normas asociadas a las aplicaciones informáticas médicas que incluyen IA, como la ISO/IEC 42001 sistema gestión AI, la BSI AAMI 34971 riesgos AI, … por la ISO/IEC JTC 1/SC42
Y también tenemos las actualizaciones de las guías de documentación técnica de software de Team-NB, de FDA y de IG-NB …
Las aplicaciones de software médico y las aplicaciones de software que incluyen inteligencia artificial han provocado un avance disruptivo en los diagnósticos y tratamientos sanitarios. En esta formación revisamos sus requisitos como producto sanitario incluyendo la nueva normativa asociada a interoperabilidad, ciberseguridad, integridad de datos y protección de datos.
Disponible ahora la versión grabada de la realizada en fecha: 18 Enero 2024
![]()
Felices Navidades !!! os deseamos desde @tecno_med
Formación «2401 – SOFTWARE MÉDICO e INTELIGENCIA ARTIFICIAL» – 18 En 2024 9h-14h con las novedades normativas y de guías
Este diciembre se aprobó el texto de la AIA Artificial Intelligence Act que incluye al software médico con IA como crítico y también diversas normas asociadas a las aplicaciones informáticas médicas que incluyen IA, como la ISO/IEC 42001 sistema gestión AI, la BSI AAMI 34971 riesgos AI, … por la ISO/IEC JTC 1/SC42
Y también tenemos las actualizaciones de las guías de documentación técnica de software de Team-NB, de FDA y de IG-NB …
Las aplicaciones de software médico y las aplicaciones de software que incluyen inteligencia artificial han provocado un avance disruptivo en los diagnósticos y tratamientos sanitarios. En esta formación revisamos sus requisitos como producto sanitario incluyendo la nueva normativa asociada a interoperabilidad, ciberseguridad, integridad de datos y protección de datos.
Fecha: 18 Enero 2024, 9h a 14h en webinar en directo y 25h en teleformación
Esperamos verte ahi … ![]()
La @AEMPS participa en JAMS 2 apoyo técnico de la CE para fortalecer la evaluación de tecnologías sanitarias

Esta iniciativa JAMS 2.0, dentro del programa EU4Health de la CE, busca mejorar la coordinación europea, la vigilancia y el control del mercado de los productos sanitarios y productos sanitarios para diagnóstico in vitro
La Agencia participa en cuatro de los ocho paquetes de trabajo y lidera uno de ellos En un periodo de tres años, las autoridades competentes de la UE, entre ellas la AEMPS, llevarán a cabo 60 inspecciones conjuntas a fabricantes y otros operadores económicos de la UE en este campo 

#IMDRF publica su guia global de etiquetado de productos sanitarios «Principles of Labeling for Medical Devices and IVD Medical Devices»
Interesante este documento de IMDRF como siempre, incluye:
– Principles for Medical Device and IVD Medical Device Identification
– General Labeling Principles for Medical Devices and IVD Medical Devices. Labeling, Label, Instructions for Use
– General Labeling Principles for Medical Devices other than IVD Medical Devices. Labeling, Label, Instructions for Use
– General Labeling Principles for IVD Medical Devices. Labeling, Label, Instructions for Use
– Labeling Principles for Medical Devices Containing Software or Software as a Medical Device
– Labeling Principles for Medical Devices and IVD Medical Devices Intended for Use by Lay Persons
– Labeling Principles for Information Intended for the Patient. 

La @AEMPS publica el plan de trabajo para 2024
Este plan que despliega de los cinco objetivos estratégicos dentro de los cinco objetivos estratégicos descritos en su Plan Estratégico 2023-2026
Incluye elementos de gran interés para los productos sanitarios:
– Mantener el plazo medio de emisión de certificados de exportación de productos sanitarios.
– Dar respuesta a las consultas relativas a la nueva extensión de los periodos transitorios del MDR y del IVDR.
– Implementar el módulo de la aplicación informática IPS (Instalaciones de Productos Sanitarios) para la presentación de comunicaciones de fabricación de productos sanitarios in house.
– Finalizar el desarrollo del registro de comercialización en España de productos sanitarios.
– Publicar las instrucciones para la comunicación de las actividades sobre re-etiquetado de productos sanitarios
– Mantener la participación en las actividades relacionadas con productos sanitarios.
– Potenciar la participación en los siguientes foros, comités o grupos de trabajo nacionales e internacionales: Grupo ICMRA (International Coalition of Medicines Regulatory Authorities). Grupo de trabajo evidencia clínica de productos sanitarios in vitro del IMDRF (International Medical Device Regulators Forum). Grupo MDCG (Medical Devices Core Group). Grupo de desabastecimiento del CAMD (Competent Authorities of Medical Devices).
– Integrar las aplicaciones nacionales con la base de datos europea de productos sanitarios EUDAMED.
La Comisión Europea publica una encuesta sobre EUDAMED Information Centre
@COCIR ( @FENIN_es ) publica su decálogo de 5 prioridades para 2024-2029 «Priority Actions on Healthcare»
Interesante publicación que nos da la visión de la industria sobre prioridades para este lustro que empieza:
1 . Mantener el atractivo de la Unión Europea (UE) para la innovación
2. Apoyar un entorno jurídico y político adecuado a sus propósitos
3. Reconocer que el sector de la tecnología médica es fundamental para la salud de la población
4. Apoyar la competitividad del sector de las tecnologías médicas
5 . Liderar la lucha contra las enfermedades crónicas
nos encanta ver que coincidimos totalmente con este decálogo de 5 puntos …

La @CNMC_es publica su informe sobre el proyecto de Real Decreto por el que se regula la publicidad de productos sanitarios de @AEMPSgob
Siguiendo el proceso legislativo que incluye consultas a diversas entidades en general no vinculantes, la CNMC publica su informe.
En el incluye su recomendación de eliminar la venta exclusiva en farmacias de productos sanitarios IVD (ya incluida en anteriores informes y por tanto sin recorrido),
otro punto que destaca es la inclusión de la restricción de los «influencers» (usuarios de especial relevancia, como se denominan legislativamente) y advierte que están regulados también por la Ley 13/2022 General de Comunicación Audiovisual LGCA articulo 94 que establece la necesidad de una reglamentación adicional en proceso de aprobación por RD que establece los requisitos para ser considerado influencer en España. (a esperar pues la definición de influencer …)
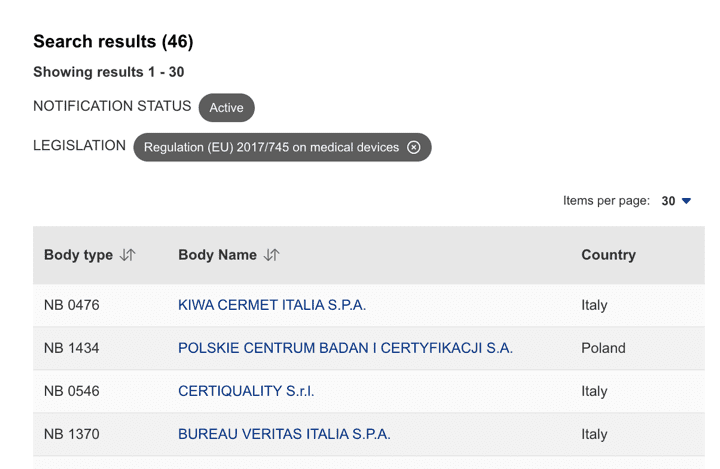
Organismos Notificados MDR (46): AFNOR CERTIFICATION (Francia) ON num. 0333 nuevo Organismo Notificado. Enhorabuena !!!
Nueva designación del Organismo Notificado:
AFNOR Certification
11 rue Francis de Pressensé
93571 La Plaine Saint-Denis Cedex France
Tel: +33 (0)1 41 62 60 98
mail: marquage-ce@afnor.org
website: https://www.afnor.org
puedes ver la lista siempre actualizada en la base de datos NANDO:
https://webgate.ec.europa.eu/single-market-compliance-space/#/notified-bodies/notified-body-list?filter=legislationId:34,bodyTypeId:3,notificationStatusId:1
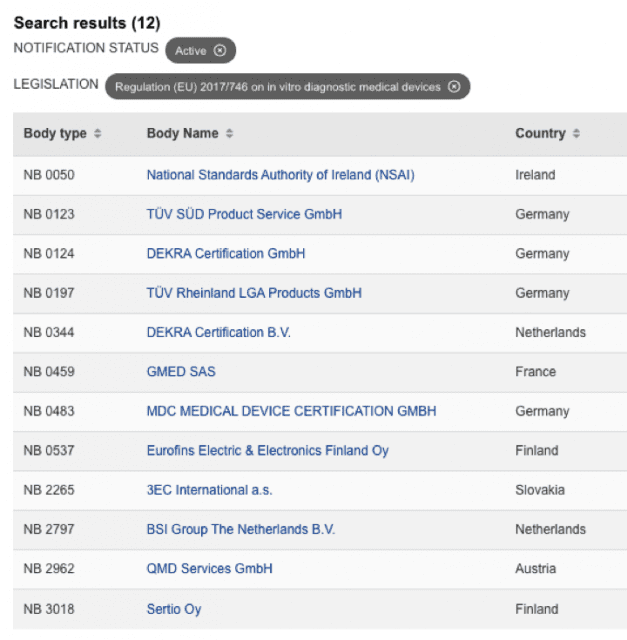
y para IVDR …
lista actualizada IVDR en:
https://webgate.ec.europa.eu/single-market-compliance-space/#/notified-bodies/notified-body-list?filter=legislationId:35,bodyTypeId:3,notificationStatusId:1

Aprobado por el Parlamento Europeo, la creación del Espacio Europeo de Datos Sanitarios ahora pasa al Consejo y después se publica entrando en vigor y se aplica a los 2 años
24 Abril 2024. El Parlamento Europeo ha respaldado la creación del EEDS (EHDS) aprobando el acuerdo interinstitucional que permitirá:
• Acceso desde cualquier país de la UE al historial médico, incluidas recetas, pruebas e imágenes médicas (basándose en la infraestructura MyHealth@EU),
• Datos sanitarios anónimos se compartirán para fines de investigación, por ejemplo, sobre enfermedades raras (muy importante para investigación)
• Sólidas salvaguardas de privacidad regularán cómo y para qué pueden compartirse datos confidenciales
No se permitirá el uso secundario con fines comerciales, incluida la publicidad, la evaluación de solicitudes de seguros o condiciones de préstamo o la toma de decisiones en el mercado laboral. Las condiciones de acceso a los datos serán tomadas por los organismos nacionales.
Próximos pasos: El Consejo adoptará ahora formalmente el Reglamento. Entrará en vigor a los 20 días de su publicación en el Diario Oficial de la Unión Europea. Su fecha de aplicación es dos años después